Получение инсулина.
Инсулин – гормон поджелудочной железы, регулирующий углеводный обмен и поддерживающий нормальный уровень сахара в крови. Недостаток этого гормона в организме приводит к одному из тяжелейших заболеваний – сахарному диабету, который как причина смерти стоит на третьем месте после сердечно-сосудистых заболеваний и рака. Инсулин – небольшой глобулярный белок, содержащий 51 аминокислотный остаток и состоящий из двух полипептидных цепей, связанных между собой двумя дисульфидными мостиками. Синтезируется он в виде одноцепочного предшественника – проинсулина, содержащего концевой сигнальный пептид (23 аминокислотных остатка) и 35-звенный соединительный пептид (С-пептид). При удалении сигнального пептида в клетке образуется проинсулин из 86 аминокислотных остатков, в котором А и В-цепи инсулина соединены С-пептидом, обеспечивающим им необходимую ориентацию при замыкании дисульфидных связей. После протеолитического отщепления С-пептида образуется инсулин.
Известно несколько форм сахарного диабета. Самая тяжёлая форма, для лечения которой больному необходим инсулин (инсулинзависимая форма заболевания), вызвана избирательной гибелью клеток, синтезирующих этот гормон (клетки островков Лангерганса в поджелудочной железе). Форма сахарного диабета, для лечения которой инсулин не требуется, распространена чаще, с ней удаётся справляться с помощью соответствующих диет и режима.
Обычно поджелудочная железа крупного рогатого скота и свиней не используется в мясной и консервной промышленности и поставляется в вагонах-рефрижераторах на фармацевтические предприятия, где проводят экстракцию гормона. Для получения 100 г кристаллического инсулина необходимо 800-1000 г исходного сырья.
Синтез обеих цепей и соединение их дисульфидными связями для получения инсулина были проведены в 1963 и 1965 гг тремя коллективами исследователей в США, Китае и Германии. В 1980 г датская компания «Ново индастри» разработала метод превращения инсулина свиньи в инсулин человека путём замещения 30-го остатка аланина в цепи В на остаток треонина. Оба инсулина не различались по активности и длительности действия.
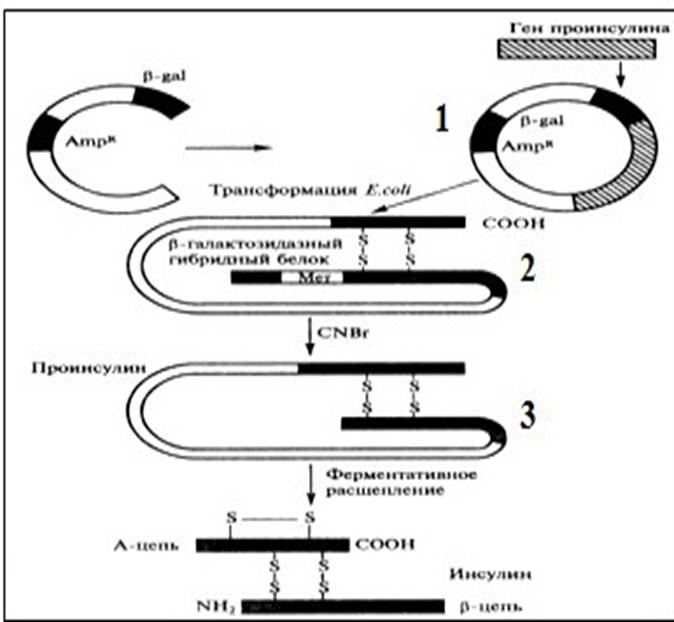
Работы по генно-инженерному получению инсулина начались около 30 лет назад. В 1978 году появилось сообщение о получении штамма кишечной палочки, продуцирующего крысиный проинсулин (США). В этом же году были синтезированы отдельные цепи человеческого инсулина посредством экспрессии их синтетических генов в клетках E. Coli (рис. 8.21):
1. Каждый из полученных синтетических генов подстраивался к 3'-концу гена фермента в-галактозидазы и вводился в векторную плазмиду - pBR322 (1).
2. Клетки E. Coli, трансформированные такими рекомбинантными плазмидами, производили гибридные (химерные) белки, состоящие из фрагмента в-галактозидазы и А и В пептида инсулина, присоединённого к ней через остаток метионина (2).
3. После обработки химерного белка бромцианом и протеолитического отщепления С-пептида образуется инсулин.
Поможем написать любую работу на аналогичную тему

