Природные газы – это вещества, которые при нормальных условиях находятся в газообразном состоянии. Углеводородные газы в пластовых условиях могут находиться в залежи в различных состояниях – газообразном, жидком или в виде газожидкостных смесей. Если газовая шапка в нефтяной залежи отсутствует, то весь газ залежи растворён в нефти. Этот газ будет, по мере снижения давления, выделятся из нефти при разработке месторождения и будет называться попутным. Состав природных газов: Природные газы, добываемые из газовых, газоконденсатных и нефтяных месторождений, состоят из углеводородов (СН4 – С4Н10, и выше), а также неуглеводородных компонентов (H2S, N2, CO, CO2, Ar, H2, He и др.). При нормальных и стандартных условиях в газообразном состоянии существуют только углеводороды С1–С4.  Углеводороды С5 и выше при нормальных условиях находятся в жидком состоянии. Газы, добываемые из чисто газовых месторождений, содержат более 95% метана. Содержание метана на газоконденсатных месторождениях колеблется от 75 - 95%.Газы, добываемые вместе с нефтью (попутный газ) представляют собой смесь метана, этана, пропан-бутановой фракции (сжиженного газа) и газового бензина. Содержание метана изменяется от 35 - 85%. Содержание тяжёлых углеводородов в попутном газе варьируется в диапазоне 20-40% , реже доходит до 60%. Нефтяной газ при н.у. содержит неполярные углеводороды - смесь углеводородов от С1 до С4: метан, этан, пропан, изо-бутан и н-бутан.
Углеводороды С5 и выше при нормальных условиях находятся в жидком состоянии. Газы, добываемые из чисто газовых месторождений, содержат более 95% метана. Содержание метана на газоконденсатных месторождениях колеблется от 75 - 95%.Газы, добываемые вместе с нефтью (попутный газ) представляют собой смесь метана, этана, пропан-бутановой фракции (сжиженного газа) и газового бензина. Содержание метана изменяется от 35 - 85%. Содержание тяжёлых углеводородов в попутном газе варьируется в диапазоне 20-40% , реже доходит до 60%. Нефтяной газ при н.у. содержит неполярные углеводороды - смесь углеводородов от С1 до С4: метан, этан, пропан, изо-бутан и н-бутан.
Плотность смеси газов рассчитывается следующим образом:
![]()
Ni – мольная доля. Плотность газа можно рассчитать через отношение молекулярной массы газа (Mi) к мольному объему (Vм).для н.у.:
![]()
Относительная плотность газа: rсм(отн)=rсм/rвозд. Для (н.у.) ρвозд=1,293; для (с.у.)ρвозд=1,205. Для идеальных газов давление смеси равно сумме парциальных давлений компонентов (закон Дальтона): P=åpi; где Р–давление смеси газов; рi–парциальное давление i-го компонента в смеси. Аддитивность парциальных объёмов компонентов газовой смеси выражается законом Амага: Vi=Ni*V; где V – объём смеси газов; Vi – объём i-го компонента в смеси.
Состояние газа при н.у. и с.у. характеризуется уравнением состояния Менделеева-Клайперона:
![]()
где Р – абсолютное давление, Па; V – объём,м3;Q–количество вещества, кмоль; с учетом отклонения поведения реального газа от идеального состояния
![]()
Коэффициент z зависит от Р и Т (приведенных критических давлений и температуры), природы газа.
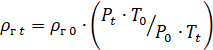
Поможем написать любую работу на аналогичную тему

