Термодинамика. Работы Майера, Джоуля, Гельмгольца позволили выработать так называемый. “закон сохранения сил” ( понятия «сила» и «энергия» в то время еще строго не различались). Однако первая ясная формулировка этого закона была получена физиками Р. Клаузиусом и У. Томсоном (лордом Кельвином) на основе анализа исследования работы тепловой машины, которое провел С. Карно. Рассматривая превращения теплоты и работы макроскопических системах С. Карно фактически положил начало новой науке, которую Томсон впоследствии назвал термодинамикой. Термодинамика ограничивается изучением особенностей превращения тепловой формы движения в другие, не интересуясь вопросами микроскопического движения частиц, составляющих вещество.
Термодинамика, таким образом, рассматривает системы, между которыми возможен обмен энергией, без учета микроскопического строения тел, составляющих систему, и характеристик отдельных частиц. Различают термодинамику равновесных систем или систем, переходящих к равновесию (классическая, или равновесная термодинамика) и термодинамику неравновесных систем (неравновесная термодинамика). Классическая термодинамика чаще всего называется просто термодинамикой и именно она составляет основу так называемой Термодинамической Картины Мира (ТКМ), которая сформировалась к середине 19 в. Неравновесная термодинамика получила развитие во второй половине 20-го века и играет особую роль при рассмотрении биологических систем и феномена жизни в целом.
Таким образом, при исследовании тепловых явлений выделились два научных направления:
1. Термодинамика, изучающая тепловые процессы без учета молекулярного строения вещества;
2. Молекулярно-кинетическая теория (развитие кинетической теории вещества в противовес теории теплорода);
Молекулярно-кинетическая теория. В отличие от термодинамики молекулярно-кинетическая теория характеризуется рассмотрением различных макроскопических проявлений систем как результатов суммарного действия огромной совокупности хаотически движущихся молекул. Молекулярно-кинетическая теория использует статистический метод, интересуясь не движением отдельных молекул, а только средними величинами, которые характеризуют движение огромной совокупности частиц. Отсюда второе название молекулярно-кинетической теории – статистическая физика.
Первое начало термодинамики. Опираясь на работы Джоуля и Майера, Клаузнус впервые высказал мысль, сформировавшуюся впоследствии в первое начало термодинамики. Он сделал вывод, что всякое тело имеет внутреннюю энергию U . Клаузиус назвал ее теплом, содержащимся в теле, в отличие от “тепла Q, сообщенного телу”. Внутреннюю энергию можно увеличить двумя эквивалентными способами: проведя над телом механическую работу -А, или сообщая ему количество теплоты Q.
D U = Q - A
В 1860 г. У. Томсон окончательно заменив устаревший термин “сила” термином “энергия”, записывает первое начало термодинамики в следующей формулировке:
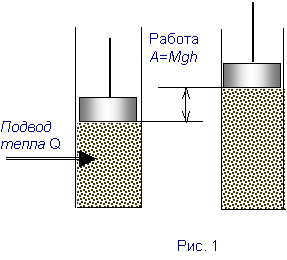
Количество теплоты, сообщенное газу, идет на увеличение внутренней энергии газа и совершение газом внешней работы (рис.1).
Q = D U + A
Для бесконечно малых изменений имеем
dQ =d U + d A
Первое начало термодинамики, или закон сохранения энергии, утверждает баланс энергии и работы. Его роль можно сравнить с ролью своеобразного «бухгалтера» при взаимопревращения различных видов энергии друг в друга.
Если процесс циклический, система возвращается в исходное состояние и U1 = U2 , a dU = 0. В этом случае все подведенное тепло идет на совершение внешней работы. Если при этом и Q = 0, то и А = 0, т.е. невозможен процесс, единственным результатом которого является производство работы без каких-либо изменений в других телах, т.е. работа «вечного двигателя» (perpetuum mobile).
Майер в своей работе составил таблицу всех рассмотренных им “сил” (энергий) природы и привел 25 случаев их превращений (тепло ® механическая работа ® электричество, химическая «сила» вещества ® теплота, электричество). Майер распространил положение о сохранении и превращении энергии и на живые организмы (поглощение пищи ® химические процессы ® тепловые и механические эффекты).
Эти примеры впоследствии были подкреплены работами Гесса (1840 г.), в которых исследовалось превращение химической энергии в теплоту, а также Фарадея, Ленца и Джоуля, в результате которых был сформулирован закон Джоуля-Ленца (1845) о связи электрической и тепловой энергии Q = J2Rt.
Таким образом, постепенно, на протяжении более четырех десятилетий сформировался один из самых великих принципов современной науки, приведший к объединению самых различных явлений природы. Этот принцип заключается в следующем:
Существует определенная величина, называемая энергией, которая не меняется ни при каких превращениях, происходящих в природе. Исключений из закона сохранения энергии не существует.
Поможем написать любую работу на аналогичную тему

