Все, конечно, помнят одно из простых, но весьма важных утверждений школьного курса физики, что вещество может находиться в трех агрегатных состояниях: твердом, жидком и газообразном. Тепловое движение частиц (атомов и молекул) в каждом агрегатном состоянии имеет свои особенности.
В газах обычно расстояние между атомами и молекулами значительно больше размеров молекул. На таких расстояниях силы взаимодействия между частицами практически отсутствуют. Это приводит к тому, что газы легко сжимаются (нет сил отталкивания) и обладают свойством неограниченно расширяться (занимать полностью предоставленный им объем), что равносильно отсутствию сил притяжения. Газ, в котором можно не учитывать силы взаимодействия между частицами и собственный объем частиц, называется идеальным.
В твердом теле молекулы и атомы совершают беспорядочные колебания относительно положений равновесия, в которых силы притяжения и отталкивания со стороны соседних атомов уравновешиваются, т.е. результирующая сила равна нулю. Твердые тела можно разделить на аморфные и кристаллические. В аморфных телах физические свойства (механические, тепловые, электрические, оптические) одинаковы во всех направлениях. В этом проявляется изотропность аморфных тел. Объясняется это тем, что атомы и молекулы в таких телах расположены беспорядочно. В кристаллических телах атомы и молекулы расположены в определенном порядке, поэтому физические свойства таких тел неодинаковы в различных направлениях, т.е. кристаллические тела анизотропны. Если через атомы кристалла мысленно провести линии, то получится решетка, называемая кристаллической.
Жидкости занимают промежуточное положение между твердыми телами и газами. Как показали исследования их структуры, молекулы жидкости некоторое время (т.н. время оседлой жизни) колеблются около положений равновесия. Через некоторое время они перескакивают в новые положения равновесия и колеблются относительно них. Именно эти перескоки молекул и являются причиной текучести жидкости, т.е. ее способности принимать форму сосуда. Взаимное расположение соседних молекул в жидкости в определенной степени упорядочено, но на расстоянии 3..4d, где d – диаметр молекулы, этот порядок нарушается. Вот почему говорят, что в жидкостях существует ближний порядок. ( Порядок в кристаллических телах называют дальним).
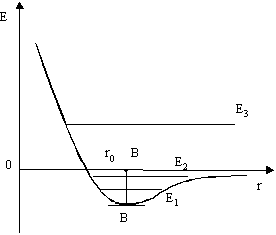
Рис. 5
Различие между жидким, твердым и газообразным состоянием можно объяснить и с энергетической точки зрения, воспользовавшись зависимостью потенциальной энергии взаимодействия молекул вещества от расстояния между ними (рис.5).
В состоянии r = r0 потенциальная энергия взаимодействия молекул минимальна.
Значения средней кинетической энергии теплового движения отложим от дна потенциальной ямы В. АВ – глубина потенциальной ямы.
Если средняя кинетическая энергия теплового движения Е1 << АВ, то частицы не могут ее преодолеть и будут совершать колебания около положения равновесия. Тело будет находиться в твердом состоянии.
Если Е ~ АВ, то молекулы будут совершать колебания с большой амплитудой и флуктуации энергии могут привести к выходу их за пределы данной потенциальной ямы и совершать колебания относительно новых положений равновесия. Это соответствует жидкому состоянию вещества.
Если Е>>АВ, то молекулы будут свободно выходить за пределы данной потенциальной ямы, почти не «ощущая» на себе ее влияния, т.е. связи с другими молекулами. Это соответствует газу.
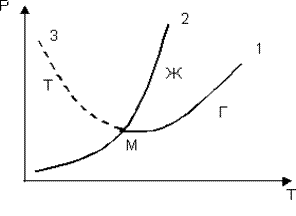
Рис. 6
Переходы вещества из одного состояния в другое называются фазовыми переходами I рода. Из сказанного выше ясно, что как агрегатное состояние вещества, так и фазовые переходы определяются внешними условиями: температурой и давлением. При высокой температуре и низком давлении мы имеем газ, при низкой температуре и высоком давлении – твердое тело. Промежуточные условия соответствуют жидкому состоянию. Графически равновесие между жидкостью и ее насыщенным паром, между жидкостью и твердым состоянием можно представить на диаграмме состояния вещества (рис.6).
Если на такой диаграмме построить для данного вещества кривые кипения, плавления и сублимации (испарения твердого вещества), то они пересекутся в одной точке М. В ней одновременно сходятся три фазы: жидкая, твердая, газообразная, поэтому эта точка называется тройной. Диаграмма состояния вещества позволяет предсказывать, в каком состоянии будет находиться вещество при различных условиях, что исключительно важно для практики.
Поможем написать любую работу на аналогичную тему

