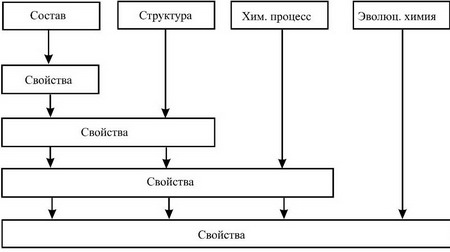
Долгое время считалось, что свойства материалов определяются, главным образом, частицами (атомами), из которых состоят тела.
Но затем стало ясно, что хотя вода и лед состоят из одних элеентов, свойства их очень различаются, и это связано с тем, как эти отдельные атомы расположены в пространстве. Было введено понятие о трех агрегатных состояниях вещества.
Но затем стало ясно, что необходимо знать и "способ приготвления" материала. Например - дамасская сталь, способ изготовления которой был утерян, или железная колонна в Дели, которая стоит уже сотни лет и не ржавеет. Современные технологии позволяют получать "металлическое стекло" (аморфную сталь), или материалы с "памятью".
Сегодня ученые обращают внимание на необычные свойства материалов, полученных природой - например, очень крепкие нити паутины или очень надежные архитектурные коралловые постройки. Поэтому современная химия пытается раскрыть эти эволюционные тайны.
Начнем более подробное обсуждение вышеозвученных положений. В основе всех подходов - частицы материалов, или, выражаясь научно - химические элементы.
Химический элемент - вид атомов с одинаковым зарядом ядра.
Но химческий элемент по разному проявляет себя в различных соединениях:
Например, водород
H2, - газ, HCl- соляная кислота, H2O - вода.
Ясно, что мы должны вспомнить все, что знаем об атомах.
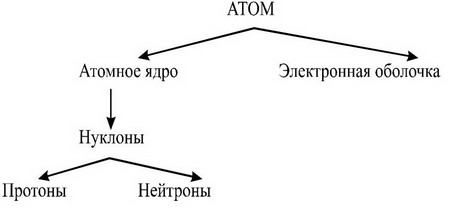

Напомним, что очень важную роль играют изотопы химических элементов.
|
Изотопы урана |
Протоны |
Нейтроны |
В земной коре, % |
|
U92234 Внимание!
Если вам нужна помощь в написании работы, то рекомендуем обратиться к
профессионалам. Более 70 000 авторов готовы помочь вам прямо сейчас. Бесплатные
корректировки и доработки. Узнайте стоимость своей работы.
|
92 |
132 |
0.0057 |
|
U92238 |
92 |
146 |
99.27 |
|
U92235 |
92 |
143 |
0.72 |
Атомы можно упорядочить, например, как это показано ниже.
Водород Z=1, 1 электрон
Гелий Z=2, 2 электрона - заполненная оболочка, инертный газ
Литий Z=3, 3 электрона, из них 2 электрона на первой оболочке, 1 электрон на второй (внешней) оболочке, активный металл.
Бериллий Z=4, 4 электрона (2+2)
Бор Z=5, 5 электронов (2+2+1) и т.д.
Но в ХIX веке гений Менделеева позволил расположить 62 известных элемента в виде периодической таблицы
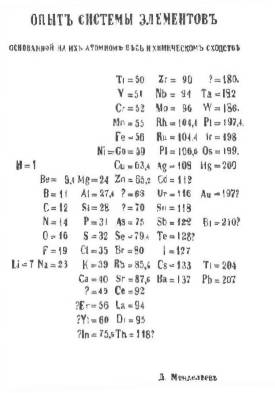
Периодическая система в своем первом варианте просто отражала существующее в природе положение дел. Как и в случае с кеплеровскими законами движения планет, таблица никак не объясняла, почему это должно быть именно так.
1930-е годы - известно 92 элемента (до урана)
Середина 1990 годов - открыто 109 элементов
(были открыты тяжелые трансурановые элементы, которые живут очень короткое время. Названия этим элементам даются в честь великих ученых: 102 элемент - нобелий, 103 - лоуренсий, 104 - курчатовий, 105 - жолиотий, 106 - резерфордий, 107 - борий, 108 - ганий, 109 - мейтнерий).
В 1999г. - открытие 114 элемента.
На сегодня известно 118 элементов
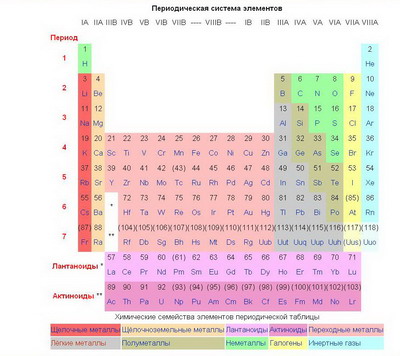
Только с появлением квантовой механики и, в особенности, принципа запрета Паули стал понятен истинный смысл расположения элементов в периодической таблице. Сегодня мы смотрим на периодическую таблицу с точки зрения того, как электроны заполняют электронные слои в атоме. Химические свойства атома (то есть то, какого рода связи будут образованы с другими атомами) определяются числом электронов в наружном слое. Так, у водорода и лития только по одному внешнему электрону, поэтому в химических реакциях они ведут себя похоже. В свою очередь, гелий и неон оба имеют заполненные внешние оболочки, и тоже ведут себя похоже, но совершенно не так, как водород и литий.
Химические элементы вплоть до урана (содержит 92 протона и 92 электрона) встречаются в природе. Начиная с номера 93 идут искусственные элементы, созданные в лаборатории. Пока самый большой заявленный учеными номер — 118. Сколько всего может быть элементов? - некоторые оценки дают цифру - 184.
От элементов перейдем к химическим соединениям.
Химическое соединение - это вещество, состоящее из атомов одного или нескольких сортов, которые объединены в частицы - молекулы, комплексы, кристаллы или иные агрегаты.
Химическая связь обусловлена обменным взаимодействием электронов (обобщение валентных электронов). Различают четыре вида химической связи:
- Ионная связь
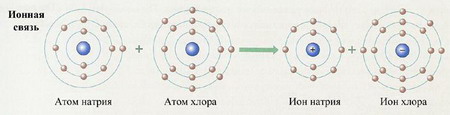
- Ковалентная связь
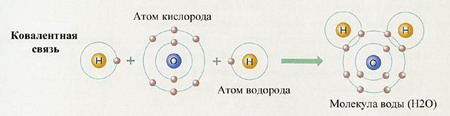
- Металлическая связь

- Водородная связь
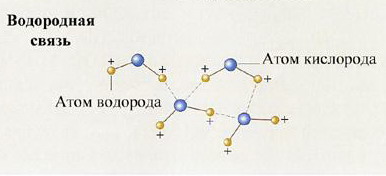
Структура или атомное строение тел. Различные состояния вещества.
Пять основных состояния вещества: плазменное, газообразное, жидкое, твердое и конденсат. Конденсат - новое состояние вещества при сверхнизких температурах - меньше 0.1 К (!!!).
Покажем, как структура (расположение атомов в пространстве) химического соединения кардинальным образом меняет свойства материала.
Рассмотрим простой одноатомный материал - углерод.
- Сажа - аморфный углерод в виде порошка, электрический изолятор.
- Графит - мягкий кристаллический материал.

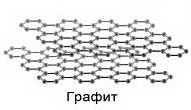
Графит очень хороший проводник электричества
- Алмаз - самый твердый кристаллический материал.

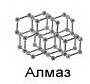
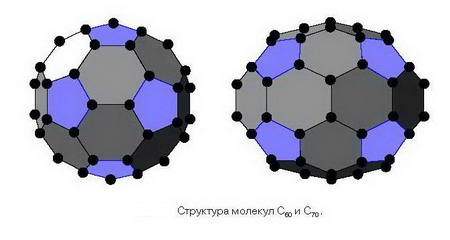
- Фуллерены - новый тип углерода.
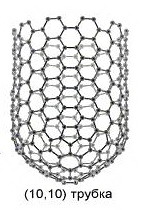
- графитовые нанотрубки - новый тип углерода.
Поможем написать любую работу на аналогичную тему

