Ковалентная связь осуществляется посредством обобществления двух валентных электронов (по одному от каждого из двух соседних атомов в молекуле). Пара обобществленных электронов принадлежит одновременно двум атомам молекулы. Электроны, образующие связь, стремятся к частичной локализации в пространстве между двумя атомами, соединенными этой связью. В этом смысле ковалентная связь характеризуется явно выраженным свойством направленности. Это хорошо видно на примере молекулы метана CH4 (рис. 1). У атома углерода четыре валентных (внешних) электрона, а каждый из атомов водорода имеет один электрон. Эти восемь электронов сосредоточены главным образом вдоль прямых, соединяющих протоны (ядра атома водорода) с ядром атома углерода.
К образованию ковалентных связей имеют тенденцию атомы III, IV и V групп периодической системы элементов. Так, углероду, кремнию и германию не хватает четырех электронов до заполнения их электронных оболочек, и поэтому атомы этих элементов могут притягиваться в основном за счет перекрытия оболочек. К веществам с ярко выраженной ковалентной связью относятся кристаллы алмаза, кремния, карбида кремния, арсенида галлия и др.
Если кристаллы с ковалентным и ионным типами связи рассматривать как предельные случаи, то между ними имеется ряд кристаллов, обладающих промежуточными типами связи.
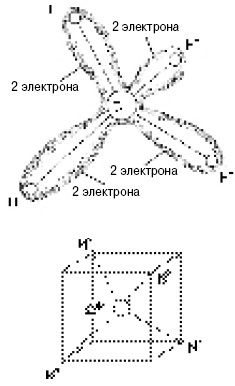
Рис. 1. Геометрия молекулы метана. Ядра водорода расположены в вершинах правильного тетраэдра, или в четырех из восьми вершин куба. Электроны сконцентрированы вдоль прямых «углерод – водород»
Поможем написать любую работу на аналогичную тему

