Основаны на создании условий, когда будущая дисперсионная среда пересыщается веществом будущей дисперсной фазы.
Различают следующие методы.
Методы физической конденсации.
I. Метод конденсации из паров.
Один из методов конденсации предложен С.З. Рогинским и А.И. Шальниковым: основан на конденсации паров в вакууме на поверхности сосуда, охлажденной жидким воздухом.
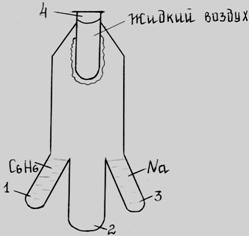
Рис.2.4. Схема прибора Рогинского и Шальникова.
В отростках 1 и 3 прибора подвергаются испарению одновременно диспергируемое вещество (например, Натрий) и дисперсионная среда (например, бензол) при Т=673К.
Пары веществ конденсируются на поверхности сосуда 4, охлаждаемого жидким воздухом до 193К – охлажденный твердый бензол содержит затвердевший Натрий. После удаления из сосуда 4 жидкого воздуха температура повышается, оттаявшая смесь бензола с натрием попадает в отросток 2 – получен коллоидный раствор натрия в бензоле.
II. Метод замены растворителя.
Растворенное вещество, оказавшись в иной среде (в которой оно не растворимо), конденсируется с образованием частиц дисперсной фазы.
Например, мастика, растворенная в спирте и внесенная в воду, в которой нерастворима, образует коллоидные частицы.
Таким образом получают золи канифоли, золи серы в воде и т.д.
По этому методу получают уретановый загуститель печатных красок и дисперсий – лапрол ДЗ.
Лапрол ДЗ представляет собой блоксополиуретан.
Макромолекула полимера состоит из участков двух типов: короткого жесткого, образованного из остатков диизоцианата и длинного гибкого, образованного из остатков простого полиэфира:
|
 |
|
||||
Нужна система растворителей, каждый из компонентов которой будет растворять отдельные фрагменты, например: спирт, гептан, вода.
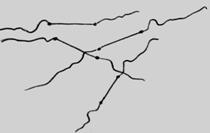
Рис. 2.5. Схема расположения макромолекул полимера в растворе.

Рис. 2.6. Схема расположения макромолекул в твердом
полимере.
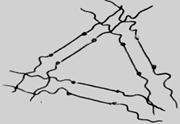
Рис. 2.7. Изменение расположения макромолекул полимера при добавлении к раствору воды (образование геля).
Методы химической конденсации.
Основаны на проведении в растворе химических реакций, сопровождающихся образованием нерастворимых или труднорастворимых веществ.
Это могут быть реакции: восстановления, окисления, разложения, гидролиза и др.
Восстановление: получают золи металлов.
Красный золь золота – реакция восстановления соли золота (аурата натрия) формальдегидом:
![]()
аурат натрия формальдегид
на образующихся частичках (микрокристаллах золота) адсорбируются ионы ![]() - потенциалобразующие ионы. Противоионы -
- потенциалобразующие ионы. Противоионы - ![]() .
.
Строение частиц можно представить схемой:
![]()
частицы золота имеют отрицательный заряд Х-.
Этим же способом можно получить из нитратов серебра (очень разбавленного раствора) желто-коричневый золь серебра.
Окисление: получают золи серы и селена действием кислорода:
![]()
строение золя серы можно представить схемой:
![]()
Разложение: получение золи серы разложением тиосульфатов и полисульфатов:
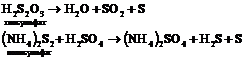
Двойной обмен: позволяет получать многие золи труднорастворимых соединений:
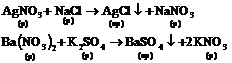
Гидролиз: получают золи гидроксидов тяжелых металлов:
![]()
Степень гидролиза возрастает с повышением температуры и с увеличением разведения.
Возможны следующие схемы строения мицелл золя:
![]()
С помощью гидролиза могут быть получены золи кремниевой, вольфрамовой, титановой и других кислот, нерастворимых в воде.
Поможем написать любую работу на аналогичную тему

