Рассмотрим термодинамическую систему, состоящую из Ф фаз и К компонентов. Предполагается, что внешние поля отсутствуют, а границы раздела фаз – плоские. Считаем, что равновесная многокомпонентная система характеризуется условиями T = const и P = const. В равновесии потенциал Гиббса имеет минимальное значение. В многофазной системе его значение складывается из энергий Гиббса отдельных фаз:
![]() (6.1)
(6.1)
![]()
При постоянных T, P находим
![]() (6.2)
(6.2)
Переход i-го компонента из фазы ![]() в фазу
в фазу ![]() можно рассмотривать как химическую реакцию
можно рассмотривать как химическую реакцию
![]()
в равновесии:
![]()
поэтому
![]()
Аналогичные равенства химических потенциалов справедливы и для всех остальных фаз и компонентов. В итоге приходим к набору условий, которые должны выполняться при равновесии:
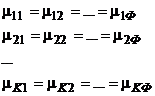 (6.2)
(6.2)
Общее число таких условий равно (Ф - 1)K. С другой стороны, минимальное число параметров, которое нужно знать, чтобы охарактеризовать гетерогенную систему равно KФ + 2 – Ф (КФ - полное число переменных Aij ; два дополнительных параметра – это полное давление и температура; Ф - число условий на концентрации в фазах, так как в любой фазе сумма мольных долей![]() ). Поэтому вариантность гетерогенной системы (число степеней свободы) равна
). Поэтому вариантность гетерогенной системы (число степеней свободы) равна
![]() (правило фаз Гиббса) (6.3)
(правило фаз Гиббса) (6.3)
Поможем написать любую работу на аналогичную тему

