Идеальным раствором называют раствор, для которого выполняется первый закон Рауля.
Идеальными при любых концентрациях являются растворы, компоненты которых близки по физическим и химическим свойствам и образование которых не сопровождается объёмными и тепловыми эффектами. В этом случае силы межмолекулярного взаимодействия между однородными и разнородными частицами примерно одинаковы, и образование раствора обусловлено лишь энтропийным фактором.
Первый закон Рауля связывает давление насыщенного пара над раствором с его составом; он формулируется следующим образом:
**Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причём коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом.
Для бинарного раствора, состоящего из компонентов А и В (компонент А считаем растворителем) удобнее использовать другую формулировку:
**Относительное понижение парциального давления пара растворителя над раствором не зависит от природы растворённого вещества и равно его мольной доле в растворе.
 В простейшем случае зависимость парциального давления пара растворителя от состава бинарного раствора имеет следующий вид:
В простейшем случае зависимость парциального давления пара растворителя от состава бинарного раствора имеет следующий вид:
![]() (V, 1)
(V, 1)
Парциальное давление растворителя в паровой фазе пропорционально его мольной доле в растворе.
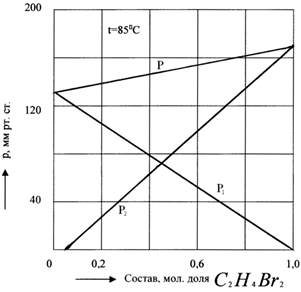
Рис.5. Общее и парциальные давления пара бинарного раствора: дибромпропан - дибромэтан. Парциальные давления на диаграмме P – x изображаются прямыми линиями.
Уравнению (V, 1) можно придать иной вид:
![]()
![]() (V, 2)
(V, 2)
Относительное понижение парциального давления растворителя в паровой фазе равно мольной доле растворенного вещества (второго компонента). Уравнения (V, 1) и (V, 2) являются выражениями закона Рауля (1886). Закон Рауля, выраженный в форме уравнения (V, 1), применим к таким растворам, насыщенный пар которых ведет себя как идеальный газ, причем лишь немногие растворы подчиняются с достаточной точностью этому закону, при любых концентрациях (т. е. при значениях x, изменяющихся в интервале от 0 до 1).
Растворы, следующие закону Рауля в форме уравнения (V, 1) при всех концентрациях и всех температурах, называются идеальными (совершенными) растворами, они являются предельным, простейшим типом жидких растворов.
Легко показать, что если для пара растворителя соблюдается уравнение (V, 1), то должно соблюдаться аналогичное уравнение для пара второго, растворенного компонента
![]() (V, 3)
(V, 3)
Уравнения (V, 1) и (V, 3) отражают свойства парциальных давлений идеальных растворов при малых давлениях. Совокупность этих уравнений носит название объединенного закона Рауля - Генри. В общем виде для многокомпонентного идеального раствора при невысоких давлениях получим:
![]()
![]() (V, 4)
(V, 4)
Уравнения (V, 1), (V, 3) и (V, 4) будут в дальнейшем изложении служить исходными для изучения термодинамических свойств идеальных растворов при небольших давлениях.
Полное давление пара идеального бинарного раствора, равное
![]() (V, 5)
(V, 5)
является также линейной функцией мольной доли.
Примерами идеальных растворов могут служить смеси (см. рис.5), бензол -толуол, бензол - дихлорэтан, гексан - октан и другие.
Составы идеального раствора и его насыщенного пара различны, т. е. ![]()
![]() х. В данном случае легко найти связь между
х. В данном случае легко найти связь между ![]() и х. В самом деле, концентрация второго компонента в паре
и х. В самом деле, концентрация второго компонента в паре ![]() . Подставив в это выражение значение P2 из закона Рауля (уравнение (V, 3)) и значение P из уравнения (V, 5), получим:
. Подставив в это выражение значение P2 из закона Рауля (уравнение (V, 3)) и значение P из уравнения (V, 5), получим:
![]()
![]() (V, 6)
(V, 6)
Отсюда видно, что ![]() = х только при равенстве давлений насыщенного пара обоих чистых компонентов, т.е. при
= х только при равенстве давлений насыщенного пара обоих чистых компонентов, т.е. при ![]() .
.
Поможем написать любую работу на аналогичную тему
Реферат
Идеальные растворы. Диаграммы равновесия пар-жидкость в бинарных системах.
От 250 руб
Контрольная работа
Идеальные растворы. Диаграммы равновесия пар-жидкость в бинарных системах.
От 250 руб
Курсовая работа
Идеальные растворы. Диаграммы равновесия пар-жидкость в бинарных системах.
От 700 руб

