Под предраковыми состояниями понимают такие патологические процессы, которые в большем или меньшем проценте случаев способны подвергаться малигнизации.
Различают облигатный (с высоким риском малигнизации) и факультативный (низкая вероятность малигнизации) предрак. К облигатным предраковым состояниям относят полипоз толстого кишечника, полипоз желудка, пигментную ксеродерму, некоторые формы мастопатии и др. Примерами факультативного предрака являются эррозии шейки матки, ряд форм фиброматозной мастопатии, аноцидный гастрит, язвенная болезнь желудка и др.
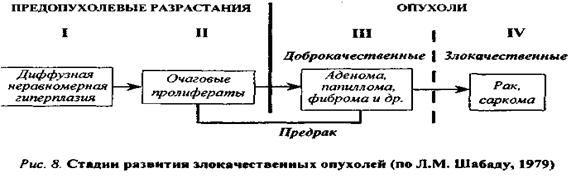
В развитии злокачественной опухоли принято выделять несколько стадий.
Первая стадия — стадия неравномерной диффузной гиперплазии, когда ткань еще полностью сохраняет нормальное строение, но заметно увеличивается численность составляющих ее элементов - клеток, волокон. Это увеличение носит диффузный характер, но неодинаково выражено в разных участках ткани; причем ограниченных участков пролиферации нет. Первая стадия еще не является предраковым состоянием. Она может быть квалифицирована как предопухолевая стадия.
Вторая стадия — стадия очаговых пролифератов. На данной стадии ткань в основном еще сохраняет нормальную структуру, но в общей массе интенсивно размножающихся клеток появляются отдельные ограниченные очаги особенно бурного размножения. Эта стадия, как и следующая за ней — третья, — стадия относительно доброкачественной опухоли (миомы, аденомы, фибромы), относится к предраковому состоянию.
Отличительной особенностью третьей стадии является все возрастающий атипизм клеток очагов пролиферации, однако, без признаков инвазивного и деструктивного роста.
Четвертая стадия — развитие злокачественной опухоли (рак, саркома). Более характерной ее чертой и является наклонность к инвазии и деструкции.
Нередко злокачественная опухоль развивается сразу же после стадии очаговых пролифератов, минуя стадию относительно доброкачественной опухоли.
Биологические особенности злокачественных новообразований:
1. Относительная автономность и нерегулируемость роста (рост не подчиняется регуляторным механизмам).
- отсутствуют лимит клеточного деления Хейблига
- ослаблены межклеточные контакты
- понижены механизмы контактного торможения
- расстройство рецепторной поверхности клеток
- нарушены синтез и чувствительность к кейлонам (вырабатываются зрелыми клетками и подавляют размножение опухолевых клеток).
- нарушена работа аденилатциклазы системы.
2. Упрощение структурно-химической организации клеток (анаплазия):
- морфологическая анаплазия
- биохимическая
- энергетическая
- функциональная
- иммунологическая
а) морфологическая:
- тканевая - соотношение стромы и паренхимы нарушены
- клеточная - разные размеры, форма клеток, миграция ядрышка, нарушение структуры поверхности клеток.
б) биохимическая анаплазия:
- набор изоферментов уменьшен
- активность ферментов снижена
- изоферментное упрощение (монотонизация)
в) энергетическая анаплазия:
энергия за счет гликолиза как анаэробного, так и аэробного.
Превалируют синтетические процессы - снижение белка за счет продуктов разрушения клеток.
г) функциональная анаплазия:
функция либо понижена, либо повышена.
Гипо- или гипертиреоз - пример.
д) иммунологическая анаплазия:
- органоспецифические антигены
- межорганные антигены.
3. Антигенное упрощение - резко уменьшено количество органоспецифических антигенов (нем. Вейлер).
4. Антигенная дивергенция - синтез. В опухолевых клетках гетерогенных антигенов (другого органа; Вейлер и Оленов).
5. Антигенная реверсия - синтез в опухолевых клетках эмбриональных антигенов (Абеленов и Татаринов - в гепатоме найден a-феропротеин; эмбриональный преальбумин в гепатоме мыши).
6. Наследуемость изменений - раковая клетка при размножении дает себе подобные.
7. Способность к метастазированию - образование вдали от первичного опухолевого узла вторичного опухолевого зачатка.
8. Нарушение соотношения гистонов и негистоновых белков.
9. Много ферментов синтеза РНК на денатурированной матрице ДНК.
РОЛЬ ИНТЕГРАТИВНЫХ СИСТЕМ ОРГАНИЗМА
Нервная система и опухолевый рост.
Исторически сначала отвергали влияние нервной системы на рост опухолей. Затем в опухолях обнаружили нервные клетки и окончания с нарушенными функциями. Руднев, Захарьин - говорили об том. Павловская лаборатория - Петрова эксперимент моделирования невроза у собак - увеличение процента возникновения опухолей. Тип ВНД имеет значение для возникновения опухоли под действием канцерогенов. нервная система влияет на окислительно-восстановительные процессы и поэтому или способствует или препятствует развитию опухолей. Опухоль легче вызвать на фоне тормозящих нервную систему средств, труднее - на фоне возбуждающих средств.
1-я стадия развития опухоли - сопровождается возбуждением, 2-я торможением в ЦНС.
Регрессия опухоли возможна в 1-ю стадию (возбуждения).
Нарушение иннервации (нейрогенная дистрофия предрасполагает к развитию опухоли) - пример с клетками опухоли Браун-Лирс, введенными в организм при денервации различных органов. Оперативное вмешательство с повреждением нервных элементов приводит к появлению отдаленных метастазов.
ЭНДОКРИННАЯ СИСТЕМА И ОПУХОЛЕВЫЙ РОСТ
По степени участия эндокринных желез в регуляции опухолевого роста:
- дисгормональные опухоли неэндокринного происхождения
- гормонально-зависимые опухоли - опухоль молочной железы - на фоне гиперэстрогенизации организма - эстрогены стимулируют процессы пролиферации в молочной железе и матке и предрасполагают к действию канцерогенов.
Фолликулостимулирующий гормон - сам стимулирует пролиферацию, стимулирует высвобождение эстрогенов.
Гипотиреоз способствует возникновению опухолей.
Гипертиреоз тормозит рецидивирование опухолей.
Тиреоидные гормоны стимулируют защитные силы организма, пролиферацию и дифференцировку (!) клеток.
Гипоталамо-гипофизарная система работает по принципу обратной связи:
недостаток йода - недостаток тиреоидных гормонов - увеличение тиреолиберинов гипоталамуса - увеличение ТТГ - увеличение пролиферации клеток щитовидной железы, в том числе опухолевых.
Опухоль влияет на гормональный профиль организма.
Опухоли щитовидной железы могут сопровождаться гипо- или гипертиреозом.
Паренеоэндокринный синдром - разновидность паренеопластического синдрома - совокупность кишечных симптомов, проявляющихся в результате действия на организм специфических и неспецифических продуктов обмена опухоли, исчезающие при ее удалении и возобновляющиеся при рецидивировании и метастазировании опухоли.
Он может быть:
нервно-трофические нарушения
аутоиммунные процессы
эндокринные нарушения
В растущей опухоли в процессе обмена образуются соединения влияющие на активность желез внутренней секреции.
В опухолях могут вырабатываться эндокриноподобные вещества.
В опухолях одной эндокринной железы могут вырабатываться гормоны другой эндокринной железы: в опухолях щитовидной железы - синтез АКТГ; в опухолях хорион-эпителиоме - синтез ТТГ.
Гормоны, вырабатываемые опухолями часто в неактивном состоянии.
ИММУННАЯ СИСТЕМА И ОПУХОЛЕВЫЙ РОСТ
Наличие иммунной реакции на опухолевые клетки. Если опухоль вызвана онкогенным вирусом, то в ней есть вирусиндуцированные антигены. В опухолях невирусного происхождения меняется антигенный спектр в результате антигенного упрощения, реверсии и т.д. При врожденном иммунодефиците - в десятки тысяч раз чаще возникают опухоли.
При трансплантации органов и применении иммунодепрессантов - кратное увеличение возникновения опухолей.
Существует иммунологический надзор в организме.
1-й эшелон защиты организма от опухоли
естественные киллеры (NK) - не требуют предварительной сенсибилизации организма антигеном:
1-я стадия - распознавание чужеродной клетки (опухолевой или пораженной вирусом)
2-я стадия - активное размножение NK
3-я стадия - контакт NK c опухолевой клеткой
4-я стадия - лизис опухолевой клетки (летальный удар)
В NK есть гранулы с перворином, которые освобождают его и в клетке-мишени образуются дыры, через которые в клетку-мишень проникает вода, клетка набухает, теряет свои отростки и погибает.
2-й эшелон защиты - макрофаги
фагоцитоз опухолевых клеток:
1 фаза - адгезия
2 фаза - захват (эндоцитоз)
3 фаза - внутриклеточное переваривание (процессинг)
Затем макрофаг объединяет свой антиген гистосовместимости группы 2 с опухолевым антигеном и выносит на своей поверхности (антигенпрезентация).
Макрофаг вырабатывает ИЛ-1, который стимулирует Т-хелпер, который вырабатывает ИЛ-2, под влиянием которого Т-клетки сенсибилизируются и тогда сенсибилизированные Т-киллеры разрушают опухолевые клетки также, как и NK.
1. Опухолевая клетка обманывает иммунную систему. При опухолевом росте синтезируются вещества супрессивного действия (активирующие Т-супрессоры в самом начале опухолевого роста.
Опухолевые клетки синтезируют хорионический гонадотропин (оказывающий супрессивное действие), В итоге в самом начале опухолевого роста иммунная система подавляется.
2. Онгстремы поместили кусочки очень злокачественной опухоли в питательную среду и добавили иммунные лимфоциты - отсутствие размножения опухоли; если добавить еще антитела - бурное размножение опухоли.
Блокады:
а) контакту лимфоцита с опухолевой клеткой препятствует двойной забор из антигенов и антител.
рецепторы лимфоцита
|
|||||||||||||||
 |
|||||||||||||||
 |
|||||||||||||||
 |
|||||||||||||||
![]() антиген опухоли лимфоцит антигены антитела
антиген опухоли лимфоцит антигены антитела
б) антиген опухоли соединяется с лимфоцитом и лимфоцит блокируется и не вступает в контакт с опухолевой клеткой.
Принципы профилактики и лечения опухолей
Общие подходы к профилактике злокачественных новообразований базируются на следующих основных методах клинической и гигиенической профилактики.
Клиническая профилактика:
а) раннее выявление и своевременное лечение предраковых состояний;
б) раннее выявление и лечение дисгормональных нарушений.
Гигиеническая профилактика — все формы борьбы:
а) за чистоту окружающей среды от канцерогенных загрязнений;
б) с вредными привычками (курение, алкоголь и др.).
В настоящее время лечение опухолевой болезни направлено на максимальное изъятие (удаление опухоли в пределах здоровых тканей) или уничтожение (химиотерапия, лучевая терапия) опухолевых клеток. С этой целью часто используется комбинированное (операция + химиотерапия; операция + лучевая терапия) и комплексное (сочетание всех трех вариантов) лечение.
В основе принципиально нового подхода к терапии рака, разрабатываемого пока экспериментаторами, лежит стремление превратить раковые клетки в здоровые путем адекватных воздействий на молекулярно-генетический аппарат бластоматозной ткани. Большие надежды возлагаются на генную инженерию.
1. Хирургическое вмешательство - удаление опухоли в пределах здоровых тканей.
2. Химиотерапия: антибиотики, цитостатики.
3. Лучевая терапия (чередовать с отдыхом).
4. Общеукрепляющие: адаптогены, витамины.
Концепция – методы генной инженерии - повернуть развитие опухолевой клетки в нормальную.
Поможем написать любую работу на аналогичную тему
Реферат
Учение о предраковых состояниях. Облигатный и факультативный предрак. Стадии развития злокачественных опухолей. Основные принципы терапии и профилактики новообразований.
От 250 руб
Контрольная работа
Учение о предраковых состояниях. Облигатный и факультативный предрак. Стадии развития злокачественных опухолей. Основные принципы терапии и профилактики новообразований.
От 250 руб
Курсовая работа
Учение о предраковых состояниях. Облигатный и факультативный предрак. Стадии развития злокачественных опухолей. Основные принципы терапии и профилактики новообразований.
От 700 руб

