Теплоемкость
определяет количество теплоты, необходимое для изменения температуры системы на ![]() К, т.е.
К, т.е. ![]() .
.
Поскольку количество теплоты ![]() , необходимое для изменения температуры системы на
, необходимое для изменения температуры системы на ![]() , зависит от характера происходящего при этом процесса, то и теплоемкость
, зависит от характера происходящего при этом процесса, то и теплоемкость ![]() системы так же зависит от процесса. Это означает, что теплоемкость является не функцией состояния системы, а функцией процесса: одна и та же система в зависимости от происходящего в ней при нагревании процесса обладает различными теплоемкостями. Численно величина
системы так же зависит от процесса. Это означает, что теплоемкость является не функцией состояния системы, а функцией процесса: одна и та же система в зависимости от происходящего в ней при нагревании процесса обладает различными теплоемкостями. Численно величина ![]() изменяется в пределах от
изменяется в пределах от ![]() до
до ![]() . Наибольшее практическое значение имеют теплоемкости
. Наибольшее практическое значение имеют теплоемкости ![]() и
и ![]() - теплоемкости для процессов при постоянном давлении и постоянном объеме. Теплоемкость величина аддитивная, поэтому в ТЕРМОДИНАМИКИ чаще используются
- теплоемкости для процессов при постоянном давлении и постоянном объеме. Теплоемкость величина аддитивная, поэтому в ТЕРМОДИНАМИКИ чаще используются
удельная теплоемкость – теплоемкость единицы массы вещества: ![]() ,
,
и соответствующие ей удельные теплоемкости при постоянном давлении ![]() и объеме
и объеме ![]() ,
,
молярная теплоемкость – теплоемкость одного моля вещества: ![]() ,
,
и соответствующие ей молярные теплоемкости при постоянном давлении ![]() и объеме
и объеме ![]() .
.
С определение теплоемкости тесно связано понятие о термостате. Термостат – тело с настолько большой теплоемкостью ![]() , что его температура при теплообмене с какой-либо системой не меняется. Когда говорят о системе помещенной в термостат, то имеют в виду систему, в которой при всех происходящих в ней процессах (расширение, намагничивание и т.д.) температура поддерживается постоянной.
, что его температура при теплообмене с какой-либо системой не меняется. Когда говорят о системе помещенной в термостат, то имеют в виду систему, в которой при всех происходящих в ней процессах (расширение, намагничивание и т.д.) температура поддерживается постоянной.
Первое начало ТЕРМОДИНАМИКИ позволяет найти значения различных теплоемкостей и установить связь между ними, если известны термическое и калорическое уравнения состояния системы.
В общем случае внутренняя энергия ![]() является функцией объема и температуры (калорическое уравнение), тогда приращение внутренней энергии, выраженное через приращение независимых переменных
является функцией объема и температуры (калорическое уравнение), тогда приращение внутренней энергии, выраженное через приращение независимых переменных ![]() .
.
Первое начало ТЕРМОДИНАМИКИ для одного моля вещества с учетом калорического уравнения состояния
 , отсюда
, отсюда
получим выражение для молярной теплоемкости:
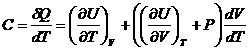 .
.
Поможем написать любую работу на аналогичную тему

