Микроинъекция ДНК в оплодотворенные яйцеклетки птиц с целью получения трансгенных линий — непростая процедура. Это связано с некоторыми особенностями воспроизводства и развития птиц. Так, при оплодотворении у птиц в яйцеклетку могут проникнуть сразу несколько сперматозоидов, а не один, как это обычно бывает у млекопитающих, и идентифицировать тот мужской пронуклеус, который соединится с женским, становится невозможно. Метод микроинъекции ДНК в цитоплазму тоже не подходит, поскольку в этом случае ДНК не интегрируется в геном оплодотворенной яйцеклетки. Наконец, даже если удастся осуществить микроинъекцию ДНК в ядро, дальнейшие операции будет трудно осуществить, поскольку у птиц яйцеклетка после оплодотворения достаточно быстро обволакивается прочной мембраной, покрывается слоем альбумина и внутренней и наружной известковыми оболочками.
Однако трансген можно вводить в область желтка (зародышевый диск), который содержит и женский, и мужской пронуклеусы и образуется раньше, чем скорлупа. После введения ДНК каждую яйцеклетку культивируют in vitro, и когда образуется зародыш, его помещают в суррогатное яйцо, чтобы имитировать вылупление. В настоящее время этот метод неэффективен и технически трудновыполним в обычных условиях.
К тому времени, когда наружная известковая оболочка яйцеклетки птиц затвердевает, зародыш, находящийся на стадии бластодермы, состоит из двух слоев по 40 000 и 80 000 клеток. Проведены эксперименты по инокуляции такого зародыша ретровирусными векторами с нарушенной репликацией, несущими бактериальные маркерные гены. В результате были получены трансгенные цыплята и обыкновенные перепела, несущие чужеродные гены в клетках зародышевой линии. Обычно такие птицы не продуцируют свободных вирусных частиц, и тем не менее применение ретровирусных векторов в качестве «поставщиков» чужеродных генов животным, которые затем могут использоваться в пищу, неизбежно вызывает вопросы относительно безопасности такого подхода.
Никаких специфичных для птиц ЕS-клеток не обнаружено, поэтому подход, основанный на их использовании, для птиц неприменим. Более перспективным представляется метод с использованием рекомбинантных эмбриональных клеток. Он состоит в следующем. Выделяют клетки бластодермы из куриного эмбриона, трансфицируют их с помощью катионных липидов (липосом), связанных с трансгенной ДНК (липосомная трансфекция), и повторно вводят в подзародышевую область свежеотложенных яиц (рис. 11). Часть потомков будет нести в каком-то небольшом количестве клетки донора: таких животных называют химерами. У некоторых химер клетки, произошедшие от трансфицированных клеток, могут образовывать линии зародышевых клеток, и после нескольких раундов скрещиваний таких химер можно получить линии трансгенных животных. Чтобы увеличить вероятность создания химер, несущих чужеродные гены в клетках зародышевой линии, число донорских клеток в химерах можно увеличить облучением эмбрионов реципиента перед введением в них трансфицированных клеток. Под действием облучения некоторые клетки бластодермы погибнут, и соотношение между трансфицированными клетками и клетками реципиента увеличится в пользу первых.
Трансгенных цыплят можно использовать для улучшения генотипа уже существующих пород — для придания им (in vivo) устойчивости к вирусным инфекциям и заболеваниям, вызываемым кокцидиями, повышения эффективности усвоения пищи, снижения уровня жира и холестерола в яйцах, повышения качества мяса. Было предложено также использовать яйцо с его высоким содержанием белка в качестве источника белковых продуктов, использующихся в фармацевтической промышленности. Экспрессия трансгена в клетках репродуктивного пути курицы, где обычно секретируется большое количество овальбумина, может способствовать накоплению соответствующего белкового продукта в яйце, откуда его можно затем выделить.
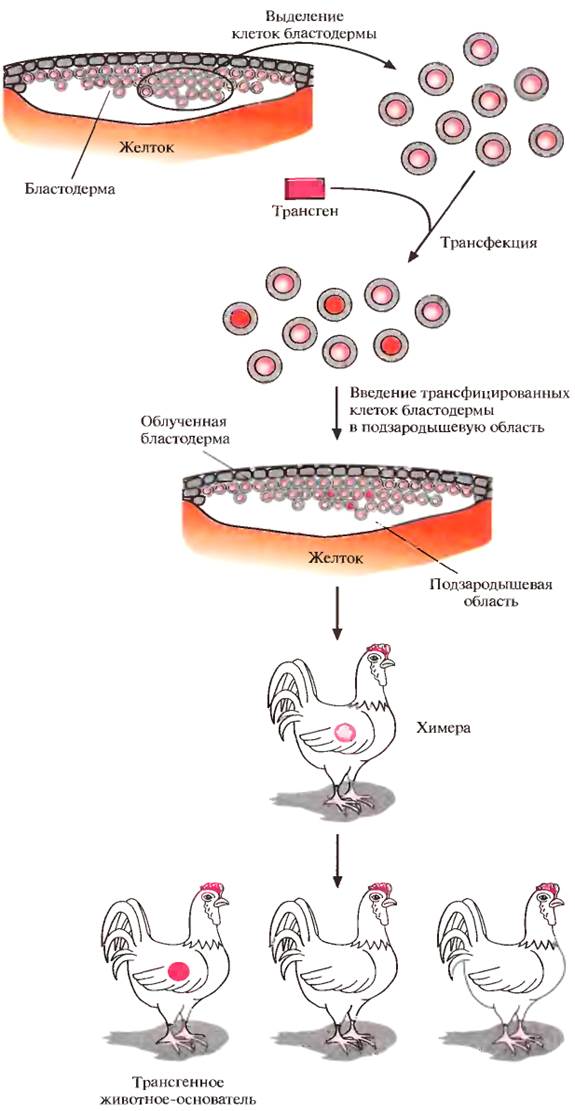
Рис. 11. Получение трансгенных цыплят трансфекцией изолированных клеток бластодермы.
Поможем написать любую работу на аналогичную тему

