В технике часто приходится встречаться с использованием двухкомпонентных (бинарных ) смесей.
Процессы с двухкомпонентными смесями исследуются посредством i, ξ- диаграммы (энтальпия — концентрация) и s, ξ-диаграммы (энтропия — концентрация), которые позволяют находить приращения энтропии, а по ним — работу разделения и потери от необратимости.
Эксергетические диаграммы позволяют определять работу разделения и эксергии компонентов смеси непосредственно.
Для этого необходимо располагать значениями е не только для различных давлений и температур, но и в зависимости от концентраций. Соответствующая эксергетическая диаграмма должна отличаться от е, t-диаграммы наличием третьей координаты ξ - концентрации .
Состояние смеси будет при этом отображаться точками в пространстве е, i, ξ.
Условиям фазовых переходов (х = 0 и, х =1, где х — влажность пара), а .также p = idem и T = idem будут соответствовать определенные поверхности.
Линии пересечения этих поверхностей с плоскостью ξ = idem дадут е, i-диаграмму для смеси соответствующего состава.
При ξ = 0 получится е, i -диаграмма чистого вещества В, при ξ = l—чистого вещества А (рис. 6.1).
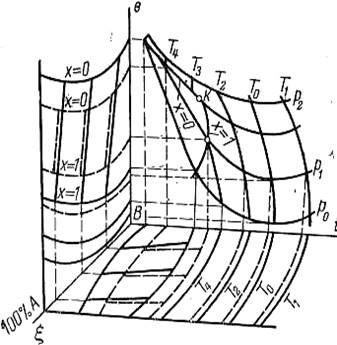
Рис.6.1 Поверхности состояний бинарной смеси в пространстве i, e, ξ
Проекции линий пересечений поверхностей Т = idem при х = 0 и х=1 с выбранными поверхностями p = idem дают на плоскостях i, ξ и е, ξ, - cоответствующие диаграммы для данных давлений p. Диаграмма i, ξ широко известна и применяется в расчетах с бинарными смесями, Диаграмма е, ξ используется для термодинамического анализа процессов с бинарными смесями, так же как и е, i-диаграмма для процессов с чистым веществом.
Обычно на диаграмму наносят кривые для ограниченного числа параметров, необходимых для расчета, чтобы не загромождать ее лишними линиями.
Посредством е, ξ -диаграммы можно находить минимальную работу процессов, включающих одновременно как разделение смеси, так и изменение любых состояний продуктов разделения, с учетом их температур и давлений.
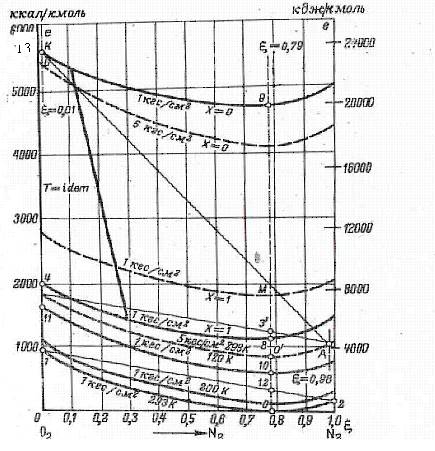
Рис..6.2 Схема расчётов процессов охлаждения и разделения на е, ξ -диаграмме
Общий вид диаграммы для воздуха с построением процессов разделения показан на рис.6.2.
Минимальная работа изменения состояния смеси равна, как и для чистого вещества, разности значений е в начальной и конечной точках процесса при ξ = idem.
Например, для воздуха ( ξ=0,78) минимальная работа охлаждения от То.с. = 293 К до Т = 110К при давлении ро.с. равна ∆е =е10 – е0 = 3120 кДж/кмоль, при охлаждении до температуры насыщения ∆е =е8 – е0 =4935 кДж/кмоль, а при охлаждении до полной конденсации ∆е =е9 – е0 = 21140 кДж/кмоль. Для чистого кислорода ( ξ =0) эти величины равны соответственно е11 – е1, е4 – е1, е13 – е1. Аналогично определяется минимальная работа и при других давлениях и концентрациях, причём начальное и конечное давления могут быть и различными.
Величина суммарной эксергии продуктов разделения находится как ордината точки пересечения прямой, соединяющей точки, соответствующие состояниям продуктов разделения, с вертикальной прямой ξ = idem заданной концентрации смеси. Расстояние по ординате ξсм от точки пересечения до точки, соответствующей состоянию исходной смеси, равно ∆е. При этом, величина минимальной работы, определяемая по диаграмме, относится к единице расхода разделяемой смеси.
Для разделения воздуха на чистые кислород (точка 1) и азот ( точка2 ) при р = рос и Т = Тос минимальная работа равна е12 – е0 = 1242 кДж/кмоль воздуха.
Приведённые примеры показывают, что расчёты и анализ процессов с использованием диаграмм могут вестись достаточно просто.
Поможем написать любую работу на аналогичную тему

