Общая черта всех процессов расширения в низкотемпературных системах – это преобразование эксергии давления ер в эксергию ет, связанную с охлаждением.
В зависимости от способа расширения такое преобразование протекает по-разному. Оно может сопровождаться отводом энергии как в форме работы (адиабатный детандер), так и в форме тепла (неадиабатная вихревая труба); отводом энергии в виде работы с одновременным подводом энергии от охлаждаемого объекта в форме тепла (неадиабатный детандер); может вообще происходить без энергетического обмена (адиабатное дросселирование).
Эксергетический метод позволяет вывести единый для всех этих процессов КПД, позволяющий сравнивать их в сопоставимых условиях.
Эффектом всех процессов расширения является эффект охлаждения. В общем виде процесс расширения при низких температурах (Т<Toc,τе < 0) показан на рис. 11.2 в координатах е-i.
Рабочее тело из состояния, соответствующего точке 1 и давлению р1, расширяется до точки 2 (давление р2); его температура снижается от Т1 до Т2.
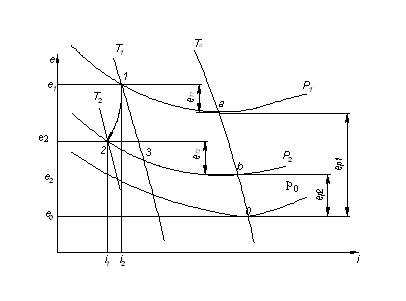
Рис.11.2. Обобщённый процесс расширения при Т<Toc
Эксергия рабочего тела уменьшалась от е1 = ет1 + ер1 до е2 = ет2 + ер2
При этом величина ер уменьшается от ер1 до ер2 величина ет возрастает от ет1 до ет2.. Такое превращение ер в ет возможно потому, что в области Т<Toc изобары имеют наклон, противоположный тому, который характерен для высокотемпературной области.
Эксергетический КПД превращения ер в ет составит:
![]() ηе = ∆ет / eр = (ет2 - ет1 ) / ( е р1 - ер2)
ηе = ∆ет / eр = (ет2 - ет1 ) / ( е р1 - ер2)
Преобразуем это уравнение к более удобному виду:
▼ eр = ер,1 - ер,2 = ▼еа,0 - ▼ еb,0 = ▼еа,b
∆ет = е Т,2 - еТ,1 = ∆е2,b - ∆е1,а = ∆еа,b - ∆е1,2
Отсюда
ηе = (∆еа,b - ∆е1,2 ) / ▼еа,b
Практически для вычисления КПД процессов расширения при Т<Toc целесообразно заменить величину ▼еа,b близкой ей величиной▼е1,3 – разностью эксергий между заданными давлениями по изотерме Т1 вместо То.с.. В этом случае
ηе = ∆е2,3 / ▼е1,3
Дросселирование
В теплотехнике сравнительно небольшое нагревание газа при дросселировании не находит технического применения, т.к. такой эффект всегда может быть получен более простым путём.
В технике низких температур охлаждение, полученное при дросселировании, служит основой большинства низкотемпературных процессов.
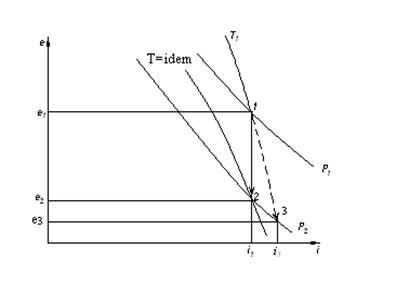
Рис.11.3. Процесс дросселирования в низкотемпературных системах, протекающий с охлаждением
На рисунке 11.3. изображен процесс дросселирования с охлаждением.
Точка 1 - начальное состояние при Т1, Р1;
Точка 2 - конечное состояние при Т2, Р2 .
При этом Т2<T1, прямая 1-2 – i = idem–процесс дросселирования.
Изменение эксергии при дросселировании определяется разностью её значений в начальной и конечной точках.
В процессе адиабатного дросселирования при отсутствии энергетического обмена работой тела с окружающей средой величина ![]() е1-2 равна потере от необратимости
е1-2 равна потере от необратимости
![]() е1-2 = е1 –е2
=d
е1-2 = е1 –е2
=d
Эксергетический КПД процесса дросселирования определяется величиной
ηе = ∆е2-3 / ![]() е1-3 ,
е1-3 ,
где т.3 определяется пересечением изотермы Т1 с изобарой р2.
Детандирование (расширение) с отдачей внешней работы.
Адиабатный детандер.
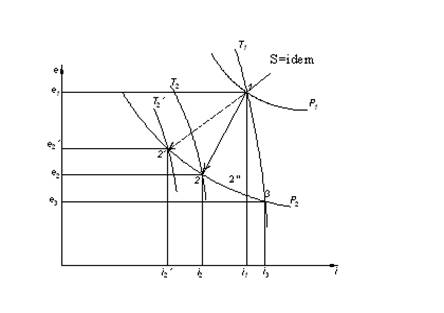
Рис.11.4. Расширение газа в адиабатном детандере
Линия 1-2′ соответствует адиабатному процессу расширения от давления Р1 до давления Р2 при условии S = idem.
Эффект охлаждения в этом предельном случае, выраженный в единицах эксергии, равен
∆е2,-3 = е2, – е3;
в количестве тепла эффект охлаждения равен
q = i2, - i3 .
Отдаваемая работа равна l = i1 - i2, .
Практически, из-за внутреннего теплообмена, трения, притока тепла извне и другим необратимым эффектам процесс в детандере протекает с увеличением энтропии и большим снижением эксергии, чем при S = idem. При этом эффект охлаждения и количество отдаваемой работы уменьшаются. Чем больше потери от необратимости, тем меньше и эффект охлаждения, и внешняя работа. В пределе процесс сведётся к дросселированию
Линия 1-3 соответствует изотермическому процессу расширения без какого либо эффекта охлаждения.
Эксергетический КПД реального детандера:
![]()
Здесь ![]() - подведенная эксергия, которая расходуется на эффект охлаждения (
- подведенная эксергия, которая расходуется на эффект охлаждения (![]() ) и внешнюю работу (l=
) и внешнюю работу (l=![]() ).
).
При условии s = const ![]() =
=![]() , числитель дроби
, числитель дроби ![]() =
=![]() и
и ![]() =1. В процессе 1-3 эффект охлаждения и внешняя работа равны нулю, поэтому
=1. В процессе 1-3 эффект охлаждения и внешняя работа равны нулю, поэтому ![]() =0
=0
Неадиабатный детандер ( αi > 0)
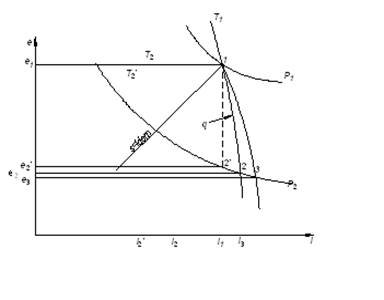
Рис.11.5.Расширение газа в неадиабатном детандере
Процесс расширения 1-2, сопровождаемый подводом тепла q от охлаждаемого объекта, в зависимости от величины q может заканчиваться на любой точке изобары P2 между линиями s==idem и T=idem. При q =0 процесс совпадает с линией s==idem (идеальный адиабатный детандер). При T=idem величина q достигает наибольшего значения (идеальный изотермический детандер).
Эксергетический КПД такой машины определяется по формуле.
![]()
Внешняя работа l не равна ![]() , поскольку процесс неадиабатный. Поэтому величина l должна быть определена или измерением или по уравнению энергетического баланса l = i1 – i2 + q
, поскольку процесс неадиабатный. Поэтому величина l должна быть определена или измерением или по уравнению энергетического баланса l = i1 – i2 + q
Поможем написать любую работу на аналогичную тему

