Живой организм и его функционирование находятся в постоянной зависимости от окружающей среды. Интенсивность обмена с внешней средой и скорость внутриклеточных процессов обмена веществ поддерживают постоянство внутренней среды и целостность организма.
Как было указано, обмен веществ в организме человека протекает не хаотично; он интегрирован и тонко настроен. Все превращения органических веществ, процессы анаболизма и катаболизма тесно связаны друг с другом. В частности, процессы синтеза и распада взаимосвязаны, координированы и регулируются нейрогормональными механизмами, придающими химическим процессам нужное направление. В организме человека, как и в живой природе вообще, не существует самостоятельного обмена белков, жиров, углеводов и нуклеиновых кислот. Все превращения объединены в целостный процесс метаболизма, подчиняющийся диалектическим закономерностям взаимозависимости и взаимообусловленности, допускающий также взаимопревращения между отдельными классами органических веществ. Подобные взаимопревращения диктуются физиологическими потребностями организма, а также целесообразностью замены одних классов органических веществ другими в условиях блокирования какого-либо процесса при патологии.
В настоящее время экспериментально обосновано существование четырех главных этапов распада молекул углеводов, белков и жиров, которые интегрируют образование энергии из основных пищевых источников. На I этапе полисахариды расщепляются до моносахаридов (обычно гексоз); жиры распадаются на глицерин и высшие жирные кислоты, а белки – на составляющие их свободные аминокислоты. Следует подчеркнуть, что указанные процессы в основном являются гидролитическими, поэтому освобождающаяся в небольшом количестве энергия почти целиком используется организмами в качестве тепла.
На II этапе мономерные молекулы (гексозы, глицерин, жирные кислоты и аминокислоты) подвергаются дальнейшему распаду, в процессе которого образуются богатые энергией фосфатные соединения и ацетил-КоА. В частности, при гликолизе гексозы расщепляются до пировиноградной кислоты и далее до ацетил-КоА. Этот процесс сопровождается образованием ограниченного числа богатых энергией фосфатных связей путем субстратного фосфорилирования. На этом этапе высшие жирные кислоты аналогично распадаются до ацетил-КоА, в то время как глицерин окисляется по гликолитическому пути до пировиноградной кислоты и далее до ацетил-КоА. Для аминокислот ситуация на II этапе несколько отлична. При преимущественном использовании аминокислот в качестве источника энергии (при дефиците углеводов или при сахарном диабете) некоторые из них непосредственно превращаются в метаболиты лимоннокислого цикла (глутамат, аспартат), другие – опосредованно через глутамат (пролин, гистидин, аргинин), третьи – в пируват и далее в ацетил-КоА (аланин, серин, глицин, цистеин). Наконец, ряд аминокислот, в частности лейцин, изолейцин, расщепляется до ацетил-КоА, а из фенилаланина и тирозина, помимо ацетил-КоА, образуется оксалоацетат через фумаровую кислоту. Как видно, II этап можно назвать этапом образования ацетил-КоА, являющегося по существу единым (общим) промежуточным продуктом катаболизма основных пищевых веществ в клетках.
На III этапе ацетил-КоА (и некоторые другие метаболиты, например α-кетоглутарат, оксалоацетат) подвергаются окислению («сгоранию») в цикле ди- и трикарбоновых кислот Кребса. Окисление сопровождается образованием восстановленных форм НАДН + Н+ и ФАДН2.
На IV этапе осуществляется перенос электронов от восстановленных нуклеотидов на кислород (через дыхательную цепь). Он сопровождается образованием конечного продукта – молекулы воды. Этот транспорт электронов сопряжен с синтезом АТФ в процессе окислительного фосфо-рилирования.
Помимо прямых переходов метаболитов этих классов веществ друг в друга, существует тесная энергетическая связь, когда энергетические потребности могут обеспечиваться окислением какого-либо одного класса органических веществ при недостаточном поступлении с пищей других. Важность белков (в частности, ферментов, гормонов и др.) в обмене всех типов химических соединений слишком очевидна и не требует доказательств. Кетогенные аминокислоты, образующие в процессе обмена ацетоуксусную кислоту (ацетоацетил-КоА), могут непосредственно участвовать в синтезе жирных кислот и стеринов.
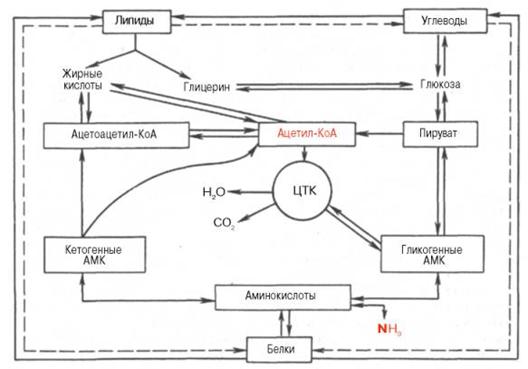
Рисунок 34 - Взаимосвязь белков, жиров и углеводов
Получены доказательства синтеза глюкозы из большинства аминокислот. Для некоторых аминокислот (аланин, аспарагиновая и глутаминовая кислоты) связь с глюконеогенезом является непосредственной, для других она осуществляется через побочные метаболические пути. Три α-кетокислоты (пируват, оксалоацетат и кетоглутарат), образующиеся соответственно из аланина, аспартата и глутамата, не только служат исходным материалом для синтеза глюкозы, но являются своеобразными кофакторами при распаде ацетильных остатков всех классов пищевых веществ в цикле Кребса для получения энергии.
Синтез незаменимых аминокислот из продуктов обмена углеводов и жиров в организме животных отсутствует. Клетки животных не содержат ферментных систем, катализирующих синтез углеродных скелетов этих аминокислот. В то же время организм может нормально развиваться исключительно при белковом питании, что также свидетельствует о возможности синтеза углеводов из белков. Процесс синтеза углеводов из аминокислот получил название глюконеогенеза. Он доказан прямым путем в опытах на животных с экспериментальным диабетом: более 50% введенного белка превращается в глюкозу. Как известно, при диабете организм теряет способность утилизировать глюкозу, и энергетические потребности покрываются за счет окисления аминокислот и жирных кислот. Доказано также, что исходными субстратами для глюконеогенеза являются те аминокислоты, распад которых сопровождается образованием прямо или опосредованно пировиноградной кислоты (например, аланин, серин, треонин и цистеин). Более того, имеются доказательства существования в организме своеобразного циклического процесса – глюкозоаланинового цикла, участвующего в тонкой регуляции концентрации глюкозы в крови в тех условиях, когда в период между приемами пищи организм испытывает дефицит глюкозы. Источниками пирувата при этом являются указанные аминокислоты, образующиеся в мышцах при распаде белков и поступающие в печень, в которой они подвергаются дезаминированию. Образовавшийся аммиак в печени обезвреживается, участвуя в синтезе мочевины, которая выделяется из организма. Дефицит мышечных белков затем восполняется за счет поступления аминокислот пищи.
Энергетическая ценность пищи оказывает определенное влияние на белковый обмен, контролируемый азотистым балансом. Так, если потребляемая энергия пищи ниже минимального уровня, то наблюдается увеличение экскреции азота, и, наоборот, при увеличении энергетической ценности пищи экскреция азота с мочой снижается.
Между циклом лимонной кислоты и орнитиновым циклом мочевино-образования имеются сложные связи, определяющие в известной степени скорость реакций, зависимую от энергетических потребностей клетки и концентраций конечных продуктов метаболизма. Как было показано, фумаровая кислота образуется в процессе распада аргинино-янтарной кислоты, синтез которой в свою очередь требует наличия аминокислоты аспартата. Образовавшаяся фумаровая кислота (из предшественника аминокислоты аспартата) далее вступает в цикл лимонной кислоты и под действием двух ферментов этого цикла: фумаратгидратазы и малатдегидрогеназы – превращается в оксалоацетат, который при участии специфической трансаминазы вновь превращается в аспартат, т.е. получается своеобразный аспартат-аргининоянтарный шунт цикла лимонной кислоты, соединенного с циклом мочевинообразования. Таким образом, при помощи этого необычного сцепленного механизма происходит переплетение реакций обоих циклов (мочевинообразования и ди- и трикарбоновых кислот).
Таким образом, скорость распада одних питательных веществ и биосинтеза других, прежде всего, определяется физиологическим состоянием и потребностями организма в энергии и метаболитах.
Поможем написать любую работу на аналогичную тему
Реферат
Взаимосвязь обмена белков, жиров и углеводов. Обмен воды и минеральных солей
От 250 руб
Контрольная работа
Взаимосвязь обмена белков, жиров и углеводов. Обмен воды и минеральных солей
От 250 руб
Курсовая работа
Взаимосвязь обмена белков, жиров и углеводов. Обмен воды и минеральных солей
От 700 руб

