Биологическое действие гормонов проявляется через их взаимодействие с рецепторами клеток-мишеней. Для проявления биологической активности связывание гормона с рецептором должно приводить к образованию химического сигнала внутри клетки, который вызывает специфический биологический ответ, например изменение скорости синтеза ферментов и других белков или изменение их активности (см. раздел 5). Мишенью для гормона могут служить клетки одной или нескольких тканей. Воздействуя на клетку-мишень, гормон вызывает специфическую ответную реакцию. Например, щитовидная железа - специфическая мишень для тиреотропина, под действием которого увеличивается количество ацинарных клеток щитовидной железы, повышается скорость биосинтеза тиреоидных гормонов. Глюкагон, воздействуя на адипоциты, активирует липолиз, в печени стимулирует мобилизацию гликогена и глюконеогенез. Характерный признак клетки-мишени - способность воспринимать информацию, закодированную в химической структуре гормона.
А. Рецепторы гормонов
Начальный этап в действии гормона на клетку-мишень - взаимодействие гормона с рецептором клетки. Концентрация гормонов во внеклеточной жидкости очень низка и обычно колеблется в пределах 10-6-10-11 ммоль/л. Клетки-мишени отличают соответствующий гормон от множества других молекул и гормонов благодаря наличию на клетке-мишени соответствующего рецептора со специфическим центром связывания с гормоном.
1. Общая характеристика рецепторов
Рецепторы пептидных гормонов и адреналина располагаются на поверхности клеточной мембраны. Рецепторы стероидных и тиреоидных гормонов находятся внутри клетки. Причём внутриклеточные рецепторы для одних гормонов, например глюкокортикоидов, локализованы в цитозоле, для других, таких как андрогены, эстрогены, тиреоидные гормоны, расположены в ядре клетки
Рецепторы по своей химической природе являются белками и, как правило, состоят из нескольких доменов.
В структуре мембранных рецепторов можно выделить 3 функционально разных участка. Первый домен (домен узнавания) расположен в N-концевой части полипептидной цепи на внешней стороне клеточной мембраны; он содержит гликозилированные участки и обеспечивает узнавание и связывание гормона. Второй домен - трансмембранный. У рецепторов одного типа, сопряжённых с G-белками, он состоит из 7 плотно упакованных α-спиральных полипептидных последовательностей. У рецепторов другого типа трансмембранный домен включает только одну α-спирадизованную полипептидную цепь (например, обе β-субъединицы гетеротетрамерного рецептора инсулина α2β2). Третий (цитоплазматический) домен создаёт химический сигнал в клетке, который сопрягает узнавание и связывание гормона с определённым внутриклеточным ответом. Цитоплазматический участок рецептора таких гормонов, как инсулин, фактор роста эпидермиса и инсулиноподобный фактор роста-1 на внутренней стороне мембраны обладает тирозинки-назной активностью, а цитоплазматические участки рецепторов гормона роста, пролактина и цитокинов сами не проявляют тирозинкиназ-ную активность, а ассоциируются с другими цитоплазматическими протеинкиназами, которые их фосфорилируют и активируют.
Рецепторы стероидных и тиреоидных гормонов содержат 3 функциональные области. На С-концевом участке полипептидной цепи рецептора находится домен узнавания и связывания гормона. Центральная часть рецептора включает домен связывания ДНК. На N-концевом участке полипептидной цепи располагается домен, называемый вариабельной областью рецептора, отвечающий за связывание с другими белками, вместе с которыми участвует в регуляции транскрипции.
Регуляция количества и активности
рецепторов
Концентрация рецепторов внутри клетки или на её поверхности и их сродство к данному гормону в норме регулируются различными способами, а также могут меняться при заболеваниях или при использовании гормонов или их агонистов в качестве лекарственных средств. Например, при воздействии β-адренергических агонистов на клетки в течение нескольких минут в ответ на новое добавление агониста прекращается активация аденилатциклазы, и биологический ответ исчезает. Такое снижение чувствительности рецептора к гормону (десенситизация) может происходить в результате изменения количества рецепторов по механизму понижающей регуляции. Гормон связывается с рецептором, комплекс гормон-рецептор путём эндоцитоза проникает в клетку (интернализуется), где часть рецепторов подвергается протеолитическому расщеплению под действием ферментов лизосом, а часть инактивируется, отделяясь от других мембранных компонентов. Это приводит к уменьшению количества рецепторов на плазматической мембране. Например, в случае инсулина, глюкагона, катехоламинов это происходит в течение нескольких минут или часов. При снижении концентрации гормона рецепторы возвращаются на поверхность клетки, и чувствительность к гормону восстанавливается. Активность рецептора, т.е. его сродство к гормону, может изменяться также в результате ковалентной модификации, главным образом путём фосфорилирования. Концентрация внутриклеточных рецепторов может также регулироваться по механизму индукции и репрессии.
По механизму действия гормоны можно разделить на 2 группы. К первой группе относят гормоны, взаимодействующие с мембранными рецепторами (пептидные гормоны, адреналин, а также гормоны местного действия - цитокины, эйкозаноиды). Вторая группа включает гормоны, взаимодействующие с внутриклеточными рецепторами.
Связывание гормона (первичного посредника) с рецептором приводит к изменению кон-формации рецептора. Это изменение улавливается другими макромолекулами, т.е. связывание гормона с рецептором приводит к сопряжению одних молекул с другими (трансдукция сигнала). Таким образом, генерируется сигнал, который регулирует клеточный ответ путём изменения активности или количества ферментов и других белков. В зависимости от способа передачи гормонального сигнала в клетках меняется скорость реакций метаболизма:
- в результате изменения активности ферментов;
- в результате изменения количества ферментов
1. Передача гормональных сигналов через мембранные рецепторы
Гормоны (первичные посредники), связываясь с рецепторами на поверхности клеточной мембраны, образуют комплекс гормон-рецептор, который трансформирует сигнал первичного посредника в изменение концентрации особых молекул внутри клетки - вторичных посредников. Вторичными посредниками могут быть следующие молекулы: цАМФ, цГМФ, ИФ3, ДАТ, Са2+, NO.
Основные этапы передачи гормональных сигналов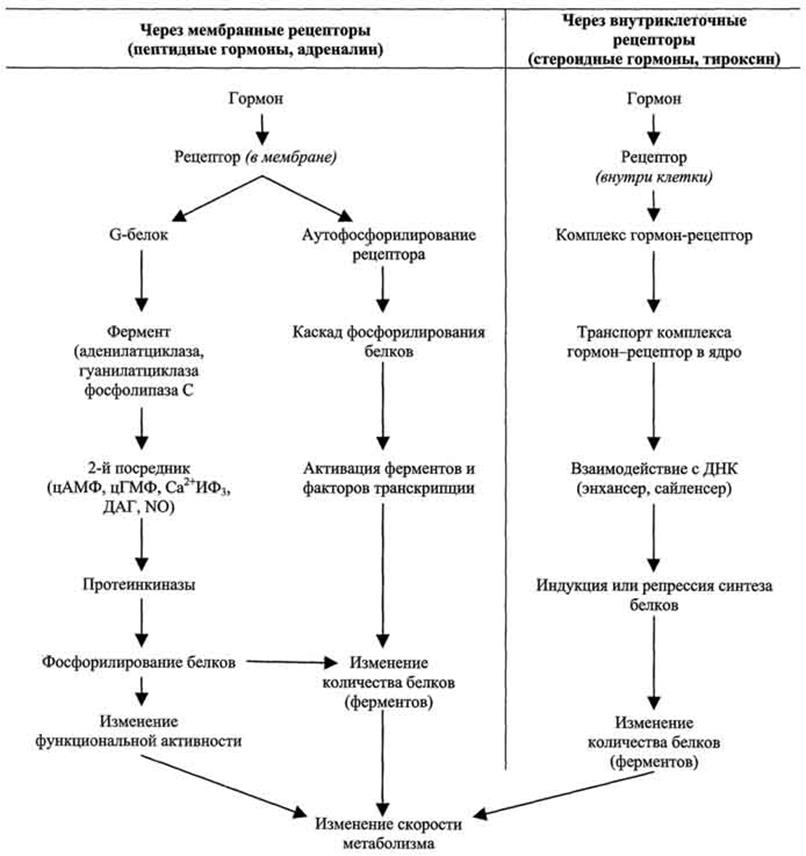
Гормоны, взаимодействие которых с рецептором клетки-мишени приводит к образованию цАМФ, действуют через трёхкомпонентную систему, которая включает белок-рецептор, G-белок и фермент аденилатциклазу. Образующийся под действием аденилатциклазы цАМФ активирует протеинкиназу А, фосфорилируюшую ферменты и другие белки (см. раздел 5). Известно более 200 различных G-белков, в структуре которых обнаружены 3 субъединицы α, β и γ (см. раздел 5). В отсутствие гормона α-субъединица G-белка связана с ГДФ. Образование комплекса гормонрецептора приводит к конформационным изменениям α-субъединицы, замене ГДФ на ГТФ и отщеплению димера βγ от α-ГТФ. В случае рецепторов, сопряжённых с Gs-белком, субъединица αs-ГТФ активирует аденилатциклазу
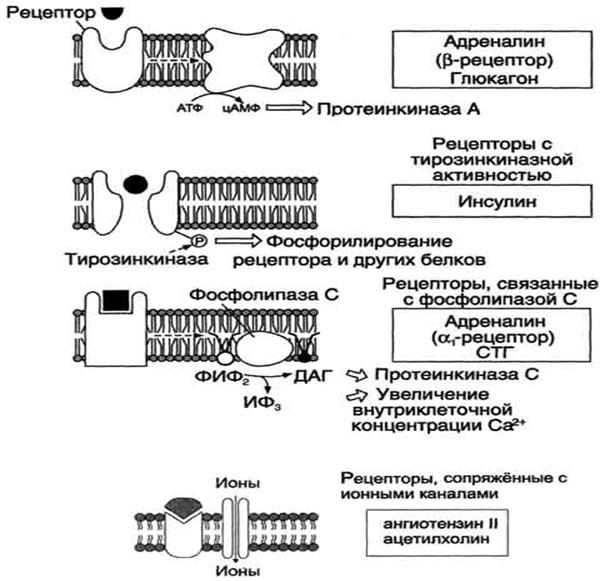
Передача гормональных сигналов через мембранные рецепторы. ИФ3 - инозитол-3-фосфат; ДАГ - диацилглицерол; ФИФ2 - фосфоинозитолбисфосфат; СТГ - соматотропный гормон. инозитоп-3-фосфат; ДАГ - диаципглицерол; ФИФ2 - фосфоинозитолбифосфат; СТГ - соматотропный гормон.
В случае рецепторов, сопряжённых с Giбелком, субъединица αi-ГТФ ингибирует аденилатциклазу. В таблице 11-4 приведены примеры гормонов, взаимодействие которых с соответствующим рецептором активирует или ингибирует аденилатциклазу.
Другая система, генерирующая цГМФ как вторичный посредник, сопряжена с гуанилатциклазой. Цитоплазматический домен такого типа рецепторов обладает активностью гуанилатциклазы, которая катализирует реакцию образования цГМФ из ГТФ> (подобно аденилатциклазе). Молекулы цГМФ могут активировать ионные каналы либо активировать цГМФ-за-висимую протеинкиназу G, участвующую в фосфорилировании других белков в клетке. Например, фосфодиэстерааа, которая гидролизует цАМФ до АМФ, активируется в результате фосфорилирования цГМФ-зависимой протеинкиназой.
Некоторые гормоны (например, вазопрессин или адреналин), образуя комплекс с соответствующими рецепторами (рецептор V1 для вазопрессина и αi-рецептор для адреналина), через активацию соответствующих G-белков активируют фосфолипазу С, в результате чего в клетке появляются вторичные посредники ИФ3, ДАГ. Молекула ИФ3 стимулирует высвобождение Са2+ из ЭР. Кальций связывается с белком кальмодулином. Этот комплекс активирует Са2+-кальмодулинзависимую протеинкиназу. Ионы кальция и ДАГ участвуют в активации протеинкиназы С
Многие гормоны передают сигнал в клетку через рецепторы, которые либо обладают тиро-зинкиназной активностью, либо связываются с цитоплазматическими белками, проявляющими активность тирозинкиназы. Связывание инсулина с мембранным рецептором, который является тирозинкиназой и имеет центр фосфорилирования, инициирует аутофосфорилирование и последующее фосфорилирование субстратов рецептора инсулина и других белков (см. разделы 5 и ниже подраздел III, Ж).
В случае взаимодействия, например, эпидермального фактора роста или инсулиноподобного фактора роста -1с мембранным рецептором сначала происходят димеризация рецептора и его активация. Активированный таким образом гомодимер рецептора, участок которого на внутренней стороне мембраны обладает активностью тирозинкиназы, фосфорилируется сам (аутофосфорилирование) и вызывает фосфорилирование других белков и ферментов, которые участвуют в активации факторов транскрипции генов.
Некоторые гормоны (например, гормон роста, пролактин, интерферон, цитокины) взаимодействуют с мембранными рецепторами, ассоциированными с цитоплазматическими протеинкиназами (так называемыми "Янус-киназами", или киназами семейства JAK). Присоединение гормона вызьшает димеризацию рецептора, присоединение Янус-киназ, их аутофосфорилирование и активацию. Янус-киназы, в свою очередь, фос-форилируют рецептор по остаткам тирозина, в результате чего рецептор связывается с другими белками, например, особыми белками - переносчиками сигнала и активаторами транскрипции (ПСАТ, или STAT - от англ, signal transducer and activator of transcription - переносчик сигнала и активатор транскрипции). Далее следует инициируемый тирозинкиназой каскад реакций фосфорилирования. Белки STAT фосфорилируются, образуют димеры, транспортируются в ядро, где, связываясь со специфическими участками ДНК, участвуют в регуляции транскрипции .
Сигнальной молекулой в клетке может служить также оксид азота NO, образующийся в организме из аргинина при участии фермента NO-синтазы, присутствующего в нервной ткани, эндотелии сосудов, тромбоцитах и других тканях .Молекула NO может быстро диффундировать через мембрану эндотелиальных клеток, где она синтезируется, в соседние клетки. Действие оксида азота кратковременно, так как Т1/2NO колеблется в пределах 5-10 с. В крови молекула существует примерно 100 мс, поскольку быстро взаимодействует с молекулярным кислородом, образуя нитрит, который далее превращается в нитрат и экскретируется с мочой. В клетках-мишенях, например, эндотелиальных клетках NO взаимодействует с входящим в активный центр гуанилатциклазы ионом железа, способствуя тем самым быстрому образованию цГМФ. Увеличение концентрации цГМФ в клетках гладких мышц вызывает активацию киназ, что в конечном итоге приводит к расслаблению ГМК сосудов и последующему их расширению. Механизм действия оксида азота объясняет использование нитроглицерина в качестве лекарственного препарата для снятия острых болей в сердце, поскольку нитроглицерин - источник образующихся молекул NO, которые и вызывают расслабление кровеносных сосудов и увеличение притока крови в миокард.
Адреналин стимулирует выведение глюкозы из печени в кровь, для того чтобы снабдить ткани (в основном мозг и мышцы) "топливом" в экстремальной ситуации. Эффект адреналина в печени обусловлен фосфорилированием (и активацией) гликогенфосфорилазы. Адреналин имеет сходный с глюкагоном механизм действия .Но возможно включение и другой эффекторной системы передачи сигнала в клетку печени
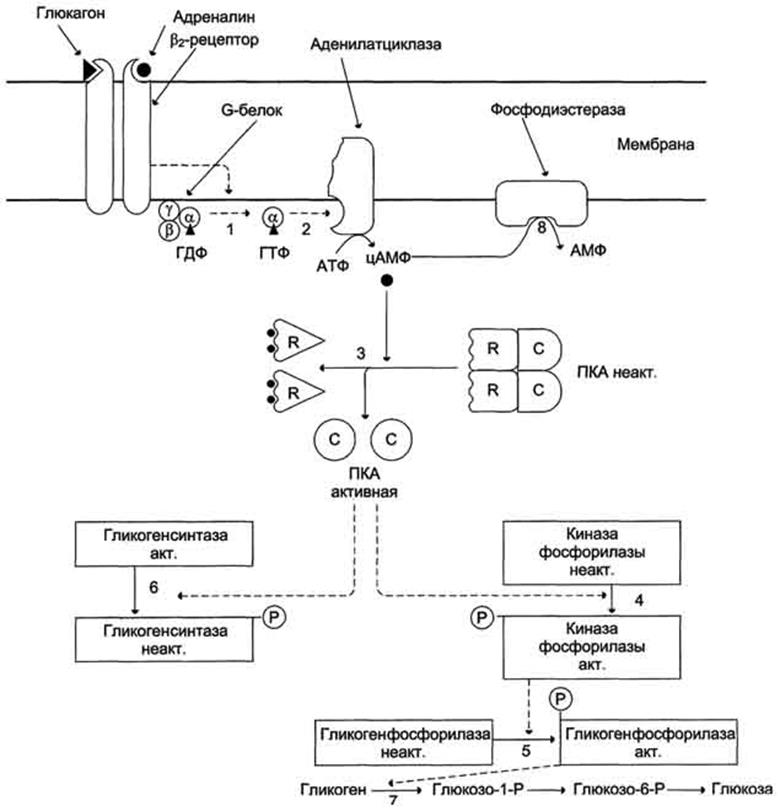
Регуляция синтеза и распада гликогена в печени глюкагоном и адреналином. 1 - глюкагон и адреналин взаимодействуют со специфическими мембранными рецепторами. Комплекс гормон-рецептор влияет на конформацию G-белка, вызывая диссоциацию его на протомеры и замену в α-субъединице ГДФ на ГТФ; 2 - α-субъединица, связанная с ГТФ, активирует аденилатциклазу, катализирующую синтез цАМФ из АТФ; 3 - в присутствии цАМФ протеинкиназа А (цАМФ-зависимая) обратимо диссоциирует, освобождая обладающие каталитической активностью субъединицы С; 4 - протеинкиназа А фосфорилирует и активирует киназу фосфорилазы; 5 - киназа фосфорилазы фосфорилирует гликогенфосфорилазу, переводя её в активную форму; 6-протеинкиназа А фосфорилирует также гликогенсинтазу, переводя её в неактивное состояние; 7 - в результате ингибирования гликогенсинтазы и активации гликогенфосфорилазы гликоген включается в процесс распада; 8 - фосфодиэсте-раза катализирует распад цАМФ и тем самым прерывает действие гормонального сигнала.
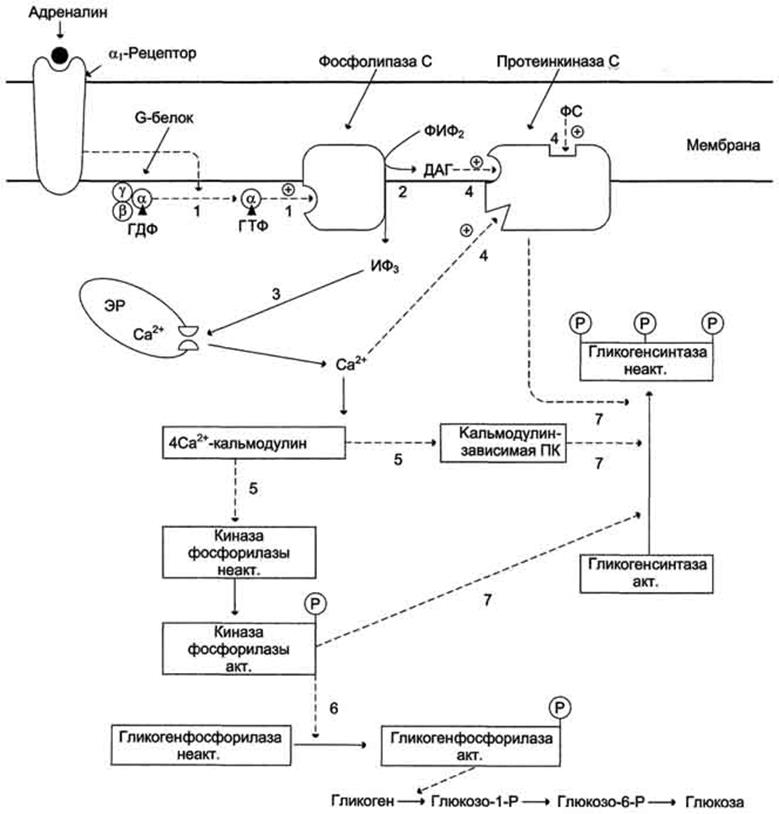
Регуляция синтеза и распада гликогена в печени адреналином и Са2+. ФИФ2- фосфатидилинозитолбисфосфат; ИФ3- инозитол-1,4,5-трифосфат; ДАГ - диацилглицерол; ЭР - эндоплазматический ретикулум; ФС - фосфодитилсерин. 1 - взаимодействие адреналина с α1-рецептором трансформирует сигнал через активацию G-белка на фосфолипазу С, переводя её в активное состояние; 2 - фосфолипаза С гидролизует ФИФ2 на ИФ3 и ДАГ; 3 - ИФ3 активирует мобилизацию Са2+ из ЭР; 4 - Са2+, ДАГ и фосфодитилсерин активируют протеинкиназу С. Протеинкиназа С фосфорилирует гликогенсинтазу, переводя её в неактивное состояние; 5 - комплекс 4Са2+-кальмодулин активирует киназу фосфорилазы и кальмодулин-зависимые протеинкиназы; 6 - киназа фосфорилазы фосфорилирует гликогенфосфорилазу и тем самым её активирует; 7 - активные формы трёх ферментов (кальмодулинзависимая протеинкиназа, киназа фосфорилазы и протеинкиназа С) фосфорилируют гликогенсинтазу в различных центрах, переводя её в неактивное состояние.
Поможем написать любую работу на аналогичную тему
Реферат
Механизм действия гормонов, связывающихся с мембранными рецепторами. Механизм регуляторного действия адреналина.
От 250 руб
Контрольная работа
Механизм действия гормонов, связывающихся с мембранными рецепторами. Механизм регуляторного действия адреналина.
От 250 руб
Курсовая работа
Механизм действия гормонов, связывающихся с мембранными рецепторами. Механизм регуляторного действия адреналина.
От 700 руб

