Трансгенные технологии могут быть использованы для выведения улучшенных пород домашних животных и птиц: коров с более высокой удойностью, овец с качественной шерстью, кур с повышенной яйценоскостью и т.п.
Эксперименты по введению чужеродных генов в клетки млекопитающих и возможность создания генетически идентичных животных путем переноса ядра из эмбриональной клетки в яйцеклетку с удаленным ядром (клонирование) позволили включать в хромосомную ДНК высших животных функциональные гены или их кластеры. Используемая стратегия состоит в следующем:
1. Клонированный ген вводят в ядро оплодотворенной яйцеклетки.
2. Инокулированные оплодотворенные яйцеклетки имплантируют в реЦипиентную женскую особь. Успешное завершение развития эмбриона млекопитающих в иных условиях невозможно.
3. Отбирают потомков, которые развились из имплантированных яйцеклеток и содержат клонированный ген во всех клетках.
4. Скрещивают животных, которые несут клонированный ген в клетках зародышевой линии и получают новую генетическую линию.
Трансгенный крупный рогатый скот. Целью трансгеноза крупного рогатого скота является изменение содержания различных веществ — белков, ферментов и других, в молоке. Например, введение трансгена белка к-казеина в клетки молочной железы и его последующая гиперэкспрессия приведет к повышению количества этого белка в молоке. Использование такого молока в качестве сырья при производстве сыра позволит значительно увеличить выход готового продукта. Введение и экспрессия гена фермента лактазы, катализирующего гидролитическое расщепление молочного сахара лактозы, даст возможность получать молоко, пригодное для людей, в организме которых нарушен синтез этого фермента.
Другой целью трансгеноза является создание домашних животных с наследственной устойчивостью к бактериальным и вирусным инфекциям, а также к паразитарным инвазиям.Для создания трансгенных коров использовали схему трансгеноза методом микроинъекций ДНК .
На первом этапе производили сбор ооцитов (женских половых клеток) у коров, забитых на бойне. Эти яйцеклетки помещали in vitro в условия, в которых происходило их созревание до стадии полной зрелости. После этого их оплодотворяли бычьей спермой. Затем производили центрифугирование оплодотворенных яйцеклеток для концентрирования желтка.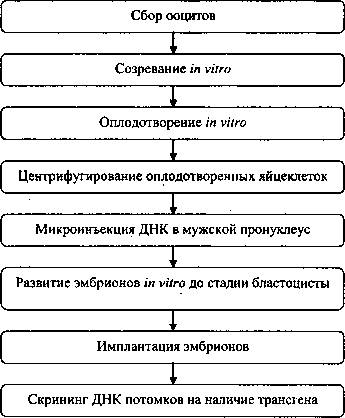
Схема получения трансгенных коров дальнейшими манипуляциями. После этого методом микроинъекции ДНК осуществляли введение трансгена в мужской пронуклеус (ядро сперматозоида); оплодотворенные яйцеклетки с генетически модифицированным геномом помещали в специальные условия in vitro, в которых начинается процесс эмбрионального развития, и культивировали до стадии бластоцисты. Эмбрион, развившийся до стадии ластоцисты, имплантировали нехирургическим путем в матку реципиентной коровы, где происходило его дальнейшее эмбриональное развитие. После рождения детенышей проводили скрининг их ДНК на наличие трансгена. На заключительном этапе производили скрещивание трансгенных особей для получения гомозиготной линии трансгенных животных. Следует отметить, что эффективность получения трансгенных животных этим методом очень низкая . Так, в экспериментах из 2407 ооцитов были получены всего два трансгенных теленка. Исследования в области усовершенствования методов трансгеноза продолжаются.
Трансгенные рыбы. Исследования в области получения трансгенных рыб касаются установления влияния трансгена гормона роста на скорость роста организма. С этой целью в яйцеклетки атлантического лосося был введен трансген, содержащий ген гормона роста лосося и регуляторную последовательность антифризного белка американской бельдюги. Как правило, трансгенные лососи были крупнее и быстрее прибавляли в весе, чем контрольные трансформированные особи. В другом эксперименте годовалые трансгенные особи нерки, полученные в результате введения в яйцеклетки генетической конструкции гормона роста, весили примерно в 11 раз больше, чем нетрансгенные. Технология получения трансгенных рыб разработана для карпа, форели, лосося и других видов рыб и состоит в следующем. Трансгены вводят в оплодотворенные яйцеклетки микроинъекцией ДНК или электропорацией. Дальнейший эмбриогенез протекает в водной среде, вне организма, в резервуарах с регулируемыми условиями. Выживаемость эмбрионов рыб после инъекций составляет от 35 до 80%, а доля трансгенных потомков — от 10 до 70%. Таким образом, эффективность трансгеноза рыб достаточно велика. Предполагается, что в будущем в рыб будут введены гены устойчивости к болезням, стрессовым воздействиям окружающей среды и др.
Таким образом, в настоящее время получены трансгенные коровы, овцы, свиньи, птицы и рыбы. Трансгены позволяют улучшать генотип пород домашнего скота и выводить породы животных с новыми признаками. Кроме того, возможно, что трансгенных домашних животных можно использовать в качестве «биофабрик» для получения продуктов клонированных генов, секретируемых в молоко.
Поможем написать любую работу на аналогичную тему

