При аэробном дыхании конечным акцептором является О2, поэтому он необходим для облигатов. Кислородное дыхание дает значительный выигрыш по энергии против брожения ианаэробного дыхания. Аэробная дыхательная цепь – достижение эволюции.
При наличии О2 у нек бактерий возникает биолюминисценция, за счет фермента люциферазы. Такие бактерии живут толко в очень чистой среде, можно использовать как биоиндикатор
О2 необходим:
- в р-циях включения О в молекулы (синтез стероидов, жирных к-т и каротиноидов)
- для начальных этапов окисления нек субстратов с помошью моно и диоксигеназ. Сами р-ции энергии не дают, но обеспечивают дальнейшие р-ции нужным в-вом.
- нужен при работе оксидаз.
- конечный акцептор е.
Как-такоевое, дыхание прокариот не отличается от процесса в митохондриях. Только про в зависимости от условий роста способны использовать другие пути, синтезируя альтернативные цитохромоксидазы. Принцип работы да и строение такое же как и у эу. В зав от субстрата и его включения в ЭТЦ, будет синтезироваться разное кол-во АТФ, тк имеются 3 пункта сопряжения. Конечный окисленный продукт – СО2, а конечный этап – ЦК. У нек есть цикл дикарбоновых к-т (кишечка), или окислительный ПФП – глюконобактер. В их случае чтобы полностью окислить гексозу цикл должен прокрутиться 6 раз.
сначала в-во должно превратиться в интермедиат ацетКоА, а потом он идет в ЦК. Для окисления белков прокариоты выделяют внеклеточные протеазы, котгидролизуют до пептидов и аминок-т. Разложение белка – аммонификация, всегда сопровождается выделением аммиака при дезаминировании к-т. При расщеплении серосодержащих вв выделяется сероводород. Аминокислоты превращаются в кеток-ты.
Метанотрофы - группа метилотрофов, способная использовать метан в качестве единственного источника как углерода, так и энергии. К ним относятся бактерии родов Methylomonas, Methylotrophus и др. Филогенетически делятся по наличию мембран-связанной и цитоплазматической метанмонооксигеназы. Фиксация формальдегида идет по рибулозомонофосфатному или сериновому пути. Возможна также фиксация экзогенного CO2.
Ключевым Е аэробных метанотрофов является метанмонооксигеназа, остальные ферменты присутствуют у других представителей метилотрофов. Восстановительные эквиваленты (CytCred) образуются только на стадиях окисления метанола и формальдегида, а образующийся на 4-й стадии NADH используется метанмонооксигеназой. Метанотрофы являются внутриклеточными симбионтами в моллюсках (Conchocele,Caliptogena) и погонофорах, живущих в метановых сипах.
Метилотрофы – аэробыанаэробы, источник урлерода и энергии – производные метана без С-С связей. ( метанол, метиламин, диметиламин, триметиламин, галометаны). Не имеют сложной системы ВЦМ. По типу питания различают три группы метилобактерий:
- Облигатные — растут только на С1-соединениях;
- Ограниченно-факультативные — используют наряду с С1-субстратами одно или несколько полиуглеродных (Сn) соединений;
- Факультативные — используют, кроме С1-соединений, широкий спектр Сn-соединений.
Также существуют метазотрофы. Это микроорганизмы, способные только окислять, либо ассимилировать, но не расти на С1-соединениях, то есть не могут использовать их одновременно как источник углерода и энергии. В последние годы установлено, что аэробные метилобактерии повсеместно распространены в природе и вносят жизненно важный вклад в биосферные циклы углерода, азота, фосфора и других биогенных макро- и микроэлементов. Наряду с метанотрофами, метилобактерии являются важнейшим звеном в цепи метаболических превращений летучих С1-соединений, также своеобразным биофильтром на их пути в тропосферу, уменьшающим опасную вероятность истощения озонового слоя Земли. В связи с тем, что растения являются глобальными продуцентами метанола на Земле метилобактерии часто ассоциированы с растениями влияя на их рост и развитие.
Уксуснокислые (ацетобактерии) - семейство из типа протеобактерий, получают энергию этанол -----ацетат. Поэтому они часто развиваются вслед за дрожжами, используя продукт спиртового брожения как субстрат для роста. Это ГОП аэробные, слабо или неподвижны. Довольно требовательны к субстратам для роста. Нуждаются в витаминах, в первую очередь в пантотеновой кислоте, но есть способные к синтезу. Ацидотолерантны, растут при рН ниже 5, хотя оптимум 5-6.
Окисляются - одноатомные спирты от 2 до 5 С, многоатомные – производные сахаров. Первые окисл до спиртов, вторые до кетонов, в альдозы и кетозы обычно. Метаболизирование сахаров идет по ПФП. Окисл субстрат варьирует в пред группы.
Аммонифицирующие – разлагают орг остатки. Бактерии гниения. Превращают органический азот в аммоний. Бациллюс, клостридиум, энтеробактерии.
Синтезируют в окр среду протеазы. Пептиды транспортируются в клетку и режутся до аминокислот, кот либо окисляются, либо используются на нужды организма.
Целлюлозоразрушающие - Аэробные бактерии - ацетивибрио, ацитомицес, алкалигенес, бациллюс, целлуломонас, эрвиния и тд. Анаэробы – бактероиды, клостридии, фибробактер и др. обычно бактерии синтезируют только часть необх Е, а потом живут бактериальным комплексом, продуцируя друг для друга в-ва.
целлюлоза гидролизуется с помошью внеклеточных целлюлаз (аэробы – грибы, миксобактерии, анаэробы – клостридии и нек грибы). Ксилан древесины и луба – гидролизуется ксиланазами до ксилозы и арабинозы. Есть соотв Е для гидролиза крахмала, пектина, хитина, лигнина и др.
гены целлюлаз и ксиланаз могут передаваться горизонтальным переносом. В клетке образуются целлюлосомы – мультиферментные комплексы гликозилгидралаз.
3. Хемосинтез. Дыхательные цепи хемолитотрофных прокариот. Группы хемолитотрофных прокариот (нитрифицирующие, тионовые, водородные бактерии, железобактерии, карбоксидобактерии).
Открыл Виноградский в 1890 г. На основе водоема с серобактериями.
Хемосинтез - тип питания, свойственный некоторым микроорганизмам и способный создавать органические вещества из неорганических ( угольной кислоты и воды) за счет знергии, получаемой при окислении ими других неорганических веществ (например, аммиака, сероводорода).
Дых цепи.
Нитрифицирующие. получают энергию в результате окисления восстановленных соединений азота ( аммиака ; азотистой кислоты ). облигатные аэробы; некоторые виды - микроаэрофилы. Большинство - облигатные автотрофы , рост которых ингибируется органическими соединениями в концентрациях, обычных для гетеротрофов . С использованием 14С-соединений показано, что облигатные хемолитоавтотрофы могут включать в состав клеток некоторые органические вещества, но в весьма ограниченной степени. Основным источником углерода остается СО2, ассимиляция которой осуществляется в восстановительном пентозофосфатном цикле . Только для некоторых штаммов Nitrobacter показана способность к медленному росту в среде с органическими соединениями в качестве источника углерода и энергии.
1 гр - окисление солей аммония до солей азотистой кислоты (нитритов) - осуществляют аммонийокисляющие бактерии (роды Nitrosomonas , Nitrosococcus , Nitrosolobus и др.):
NH4+ + 1,5O2 переходит в NO2- + Н2О + 2Н+
2 гр - окисление нитритов до нитратов - осуществляют нитритокисляющие бактерии, относящиеся к родам Nitrobacter , Nitrococcus и др.:
NO2- + 1/2*O2 переходит в NO3-
Процесс нитрификации локализован на цитоплазматической и внутрицитоплазматических мембранах. Ему предшествует поглощение NH4+ и перенос его через ЦПМ с помощью медьсодержащей транслоказы. При окислении аммиака донитрита атом азота теряет 6 электронов. Предполагается, что на первом этапе аммиак окисляется до гидроксиламина с помощью монооксигеназы, катализирующей присоединение к молекуле аммиака 1 атома О2; второй взаимодействует, вероятно, сНАД*Н2 , что приводит к образованию Н2О. Электроны от NH2OH поступают в дыхательную цепь на уровне цитохрома с и далее на терминальную оксидазу. Их транспорт сопровождается переносом 2 протонов через мембрану, приводящим к созданию протонного градиента и синтезу АТФ .
Вторая фаза нитрификации сопровождается потерей 2 электронов. Окисление нитрита до нитрата, катализируемое молибденсодержащим ферментом нитритоксидазой, локализовано на внутренней стороне ЦПМ и происходит следующим образом:
NO2- + Н2О переходит в NO3- + 2Н+ 2е
Электроны поступают на цитохром а1 и через цитохром с на терминальную оксидазу аа3, где акцептируются молекулярным кислородом ( рис. 98 , Б). При этом происходит перенос через мембрану 2Н+. Поток электронов от NO2- на О2 происходит с участием очень короткого отрезка дыхательной цепи. Восстановитель образуется в процессе энергозависимого обратного переноса электронов. Большая нагрузка на конечный участок дыхательной цепи объясняет высокое содержание цитохромов с и а у нитрифицирующих бактерий.
Многие хемоорганогетеротрофные бактерии, принадлежащие к родам Arthrobacter ,Flavobacterium , Xanthomonas , Pseudomonas и др., способны окислять аммиак ,гидроксиламин и другие восстановленные соединения азота до нитритов или нитратов . Процесс нитрификации этих организмов, однако, не приводит к получению ими энергии. Изучение природы этого процесса, получившего название гетеротрофной нитрификации, показало, что, возможно, он связан с разрушением образуемой бактериальными культурами перекиси водорода с помощью пероксидазы. Образующийся при этом активный кислород окисляет NH3 до NO3-.
Нитрифицирующие бактерии обнаружены в водоемах разного типа и в почвах, где они, как правило, развиваются совместно с бактериями, жизнедеятельность которых приводит к образованию исходного субстрата нитрификации - аммиака .
Процесс нитрификации, являясь важным звеном в круговороте азота в природе, имеет как положительные, так и отрицательные стороны. Переведение азота из аммонийной формы в нитратную способствует обеднению почвы азотом, поскольку нитраты легко вымываются из почвы. В то же время нитраты - хорошо используемый растениями источник азота. Связанное с нитрификацией подкисление почвы улучшает растворимость и, следовательно, доступность некоторых жизненно необходимых элементов, в первую очередь фосфора и железа.
Тионовые бактерии. Использование процесса окисления серы и ее неорганических восстановленных соединений для получения клеточной энергии показано для группы тионовых бактерий, представленных родами Thiobacillus , Thiomicrospira , Thiodendron и др. Это одноклеточные организмы разной морфологии и размеров; неподвижные или подвижные (движение осуществляется с помощью полярно расположенных жгутиков ); бесспоровые. Размножаются делением или почкованием. Имеют клеточную стенку грамотрицательного типа. Для некоторых представителей рода Thiobacillus характерна развитая система внутрицитоплазматических мембран.
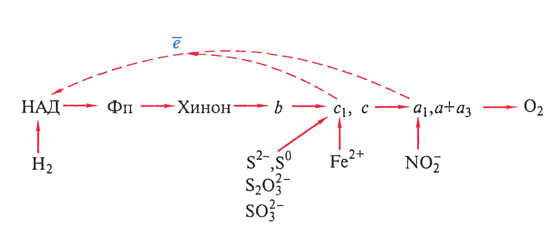
Для тионовых бактерий показана способность окислять с получением энергии помимо молекулярной серы (S0) многие ее минеральные восстановленные соединения: сульфид(S--), тиосульфат (S2O3--), сульфит (SO3--), тритионат (S3O6--), тетратионат (S4O6--). Некоторые тионовые бактерии могут получать энергию за счет окисления тиоцианата(CNS-), диметилсульфида (CH3SCH3), диметилдисульфида (CH3SSCH3), а также сульфидов тяжелых металлов. Там, где в качестве промежуточного продукта окисления образуется молекулярная сера, она откладывается вне клетки. Thiobacillus ferrooxidansполучает энергию, окисляя также двухвалентное железо.
Полное ферментативное окисление тионовыми бактериями молекулярной серы и различных ее восстановленных соединений приводит к образованию сульфата . Окисление сероводорода до сульфата сопровождается потерей 8 электронов, поступающих в дыхательную цепь, при этом в качестве промежуточных продуктов образуется молекулярная сера и сульфит:
H2S приводит к S0 приводит к SO3-- приводит к SO4--
На этапе окисления сульфита до сульфата, протекающего с образованием аденилированного промежуточного соединения денозинфосфосульфата (АФС), имеет место субстратное фосфорилирование, позволяющее запасать освобождающуюся при этом энергию в молекулах АТФ :
SO3-- + АМФ приводит к АФС + 2е;
АФС + Фн приводит к SO4-- + АДФ
Далее с помощью аденилаткиназы из АДФ синтезируется АТФ:
2АДФпереходит в АМФ + АТФ
Основное же количество энергии тионовые бактерии получают в результате переноса образующихся при окислении восстановленной серы электронов, поступающих в дыхательную цепь на уровне цитохрома а ( рис. 97 ). Дыхательная цепь тионовых бактерий содержит все типы переносчиков, характерных для аэробныххемогетеротрофов . У тионовых бактерий обнаружены флавопротеины , убихиноны ,FeS-белки , цитохромы типа b, с, цитохромоксидазы о, d, a+а3.
Некоторые виды относятся к облигатным хемолитоавтотрофам , другие - могут расти как хемолитоавтотрофно, так и хемоорганогетеротрофно , используя в последнем случае в качестве источника углерода и энергии ряд органических соединений (кислоты, сахара, спирты, аминокислоты). Наконец, описаны тионовые бактерии, растущиехемолитогетеротрофно , используя в качестве источника углерода только органические соединения, а энергию получая за счет окисления восстановленных соединений серы. Основным механизмом ассимиляции СО2 служит восстановительный пентозофосфатный цикл , обнаруженный у всех тионовых бактерий. Вспомогательную роль играют реакции карбоксилирования трехуглеродных соединений, в первую очередьфосфоенолпировиноградной кислоты .
Тионовые бактерии приспособлены к разным условиям обитания. Thiobacillus thiooxidansи Thiobacillus ferrooxidans - ярко выраженные ацидофилы (оптимальный рН 2-4),Thiobacillus denitrificans и Thiobacillus thioparus , наоборот, развиваются только в нейтральной и щелочной среде (рН 7-10). Большинство тиобацилл относятся кмезофилам с оптимальной температурой роста приблизительно 30 градусов по С. Описаны термофильные штаммы, растущие при 60-70 градусов по С.
Водородные бактерии. К водородным бактериям относят эубактерии, способные получать энергию путем окисления молекулярного водорода с участием О2, а все вещества клетки строить из углерода СО2. Таким образом, водородные бактерии - это хемолитоавтотрофы , растущие при окислении Н2 в аэробных условиях:
Н2 + 1/2*О2 переходит в Н2О
Помимо окисления для получения энергии молекулярный водород используется вконструктивном метаболизме . На 5 молекул Н2, окисленного в процессе дыхания, приходится 1 молекула Н2, затрачиваемого на образование биомассы:
6Н2 + 2О2 + СО2 переходит в СН2О + 5Н2О
Молекулярный водород - наиболее распространенный неорганический субстрат, используемый эубактериями для получения энергии в процессе окисления. Число бактерий, растущих хемолитотрофно на основе использования Н2 в качестве источника энергии, намного больше организмов, использующих для этой цели другие неорганические субстраты (восстановленные соединения серы, азота, железа).
Способность к энергетическому использованию Н2 может сочетаться с конструктивным метаболизмом облигатно гетеротрофного типа (например, у представителей родовAzotobacter или Acetobacter ) или происходить в строго анаэробных условиях (сульфатвосстанавливающие бактерии ), что не позволяет относить обладающие этими особенностями организмы к водородным бактериям. Таким образом, водородные бактерии представляют только часть эубактерий, способных использовать Н2 для получения энергии. Пути использования молекулярного водорода эубактериями суммированы в табл. 31 . Водородные бактерии характеризуются способностью сочетать конструктивный метаболизм автотрофного типа (вариант 1) с получением энергии за счет окисления Н2 с участием молекулярного кислорода (вариант 3).
Электронтранспортная цепь водородных бактерий по составу аналогична митохондриальной. Большинство из них относится к облигатным аэробам. Однако среди облигатных аэробов преобладают виды, тяготеющие к низким концентрациям О2 в среде. Особенно чувствительны к О2 водородные бактерии, растущие хемолитоавтотрофно , а также в условиях фиксации молекулярного азота. Последнее объясняется инактивирующим действием молекулярного кислорода на гидрогеназу и нитрогеназу.
все изученные водородные бактерии могут быть разделены на 3 группы. Большинство содержит только одну форму фермента - связанную с мембранами. Есть виды, содержащие обе формы или только растворимую (цитоплазматическую) гидрогеназу.
Гидрогеназы, имеющие различную локализацию, вероятно, выполняют в клетке разные функции. Связанный с мембранами фермент не способен восстанавливать НАД+ , передает электроны непосредственно в дыхательную цепь на уровне флавопротеинов ,хинонов или цитохрома b и, таким образом, имеет отношение только к энергетическим процессам. Растворимая гидрогеназа переносит электроны на молекулы НАД+, которые участвуют далее в различных биосинтетических реакциях.
Если водородные бактерии содержат обе формы гидрогеназы, функции между ними четко разделены. В случае отсутствия у водородных бактерий цитоплазматической гидрогеназы возникает проблема получения восстановителя при хемолитоавтотрофном способе их существования. Она решается с помощью механизма обратного переноса электронов на НАД+ . При функционировании только цитоплазматической гидрогеназы она выполняет обе функции: часть восстановительных эквивалентов с НАД*Н2поступает в дыхательную цепь , другая расходуется по каналам конструктивного метаболизма . Таким образом, из всех хемолитоавтотрофных эубактерий только водородные бактерии с помощью определенной формы гидрогеназы могут осуществлять непосредственное восстановление НАД+ окислением неорганического субстрата. В электронтранспортную цепь электроны, следовательно, могут поступать с НАД*Н2 или включаться на уровне переносчиков с более положительным окислительно-восстановительным потенциалом. С этим связан энергетический выход процесса: функционирование в дыхательной цепи 3 или 2 генераторов дельта мю Н+ .
Железобактерии. Бактерии получающие энергию за счет окисления Железа 2 до железа 3.
Ошибочно сюда относят бакт с инкрустацией окислами – железо в этом случае окисляется, но клеткане получает никакой энергии.
Наконец, среди железобактерий есть организмы, у которых окисление Fe++ связано с получением энергии. В этом случае отложение окислов железа служит показателем активности энергетических процессов. В нейтральной или слабокислой среде окисление Fe++ до Fe+++ происходит в результате непосредственного взаимодействия с Н2О2:
2Fe++ + Н2О2 + 2Н+ переходит в 2Fe+++ + 2Н2О
На основании морфологических характеристик все железобактерии могут быть разделены на две группы: нитчатые железобактерии и одноклеточные железобактерии .
Эубактерий, описанные в этом разделе, широко распространены в природе и могут существовать в большом диапазоне условий. Облигатные ацидофилы обнаружены в подземных водах сульфидных месторождений, кислых водах железистых источников и кислых озерах с высоким содержанием закисного железа. Нитчатые формы также занимают вполне определенные экологические ниши. Представители рода Leptothrix - обитатели олиготрофных железистых поверхностных вод, Sphaerotilus предпочитают среды с высоким содержанием органических веществ.
Карбоксидобактерии. аэробные эубактерии , способные расти, используя окись углерода (СО) в качестве единственного источника углерода и энергии. Таким свойством обладают некоторые представители родов Pseudomonas , Achromobacter ,Comamonas . (Способность окислять СО обнаружена у представителей прокариот, принадлежащих к эубактериям ( пурпурные несерные бактерии , цианобактерии ,клостридии ) и архебактериям ( метанобразующие бактерии ).
Карбоксидобактерии могут расти автотрофно , ассимилируя СО2 в восстановительном пентозофосфатном цикле , а также использовать в качестве единственного источника углерода и энергии различные органические соединения. При выращивании на среде с СО2 в качестве единственного источника углерода большинство карбоксидобактерий энергию могут получать за счет окисления молекулярного водорода.
Использование СО карбоксидобактериями происходит путем его окисления в соответствии с уравнением:
СО + Н2О переходит в СО2 + 2е + 2Н+
Продукт реакции используется далее по каналам автотрофного метаболизма. (Таким образом, при выращивании карбоксидобактерий на среде с СО в качестве единственного источника углерода и энергии источником углерода служит не СО, а СО2). Теоретически суммарное уравнение окисления СО и синтеза клеточной биомассы карбоксидобактерий может быть представлено в следующем виде:
7СО + 2,5О2 + Н2О переходит в 6СО2 + (СН2О),
где (СН2О) - символ биомассы.
Из уравнения видно, что окисление СО - неэффективный способ получения энергии. Карбоксидобактерии для синтеза клеточного вещества вынуждены окислять большое количество СО: на биосинтетические процессы в в разных условиях роста идет от 2 до 16% углерода СО.
Окисление СО карбоксидобактериями осуществляется с участием по крайней мере одного специфического фермента - СО-оксидазы. Это флавопротеин, в молекуле которого содержатся молибден и FeS-центры. Фермент в клетке находится в растворимой и связанной с мембраной форме. Растворимая СО-оксидаза локализована с внутренней стороны ЦПМ . При росте карбоксидобактерий на СО в качестве единственного источника углерода и энергии СО-оксидаза выполняет следующие функции: окисляет СО до СО2, передает электроны в дыхательную цепь и участвует в синтезе НАД*Н2 путем обратного переноса электронов.
Состав дыхательных цепей карбоксидобактерий аналогичен таковому водородных бактерий . Для карбоксидобактерий Pseudomonas carboxydovorans показано, что дыхательная цепь разветвлена на уровне убихинона или цитохрома b . Одна ветвь (органотрофная ) содержит цитохромы b558, с и а1, вторая ( литотрофная ) - цитохромы b561 и о. При окислении органического субстрата электроны поступают преимущественно в органотрофную ветвь цепи, при окислении Н2 и СО - в обе. Низкая энергетическая эффективность использования СО карбоксидобактериями указывает на то, что перенос электронов по цепи в этом случае приводит к функционированию, вероятно, 1 генератора дельта мю Н+ .
Интересно, что бакт исп в кач-ве донора в-во, служащее ингибитором терминальных оксидаз и цитохромов. Но в их ЭТЦ ничего радикально отличающегося от остальных цепей не обнаружено. Возможные механизмы устойчивости:
- быстрая детоксикация СО с помощью окисляющего фермента;
- индукция ответвляющихся от основного пути СО-нечувствительных терминальных оксидаз, через которые и осуществляется перенос электронов на О2;
- повышенный синтез компонентов электронтранспортной цепи;
- пространственное разобщение процесса окисления СО и цитохромоксидаз, чувствительных к ней.
Основными источниками окиси углерода в природных условиях являются промышленное производство, транспорт, вулканическая деятельность и биологические процессы. Известно, что СО образуется в результате жизнедеятельности разных организмов (бактерии, грибы, водоросли, животные, растения). Одним из путей удаления этого токсического соединения служит использование его бактериями, и в первую очередь в наибольшей степени приспособленными для этого.
Поможем написать любую работу на аналогичную тему

