Температура – количественная мера «нагретости» тела. Температура является мерой кинетической энергии тела. Измерение «нагретости» сводится к измерению характеристик тела, изменяющихся от «нагретости». Тело, выбирающееся для измерения «нагретости», называется термометрическим, а величина, посредством которой измеряют «нагретость» – термометрической. Температурой
называется числовое значение величины, с помощью которой характеризуется «нагретость» тела. Температура не является сама по себе термометрической величиной, которая взята за основу её измерения. Она получается из термометрической величины. Пусть ![]() и
и ![]() – термометрические величины замерзания и кипения воды соответственно,
– термометрические величины замерзания и кипения воды соответственно, ![]() и
и ![]() – температуры кипения и замерзания воды. Градусом температуры называется величина:
– температуры кипения и замерзания воды. Градусом температуры называется величина: 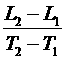 . Температура термометрического тела определяется по формуле:
. Температура термометрического тела определяется по формуле: 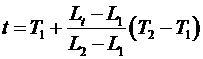 – эмпирическая шкала температур (шкала Цельсия, Фаренгейта, Реомюра).
– эмпирическая шкала температур (шкала Цельсия, Фаренгейта, Реомюра).
Газовый термометр – прибор, построенный на основе разрежённого газа. Существует зависимость ![]() , которая легко считается для идеальных газов.
, которая легко считается для идеальных газов.
Используя законы Шарля и Гей-Люссака: 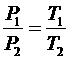 . Для воды
. Для воды
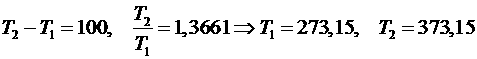 .
.
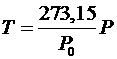 , где
, где ![]() – давление газа при температуре тройной точки,
– давление газа при температуре тройной точки, ![]() – давление при измеряемой температуре. Таким образом, переходим к абсолютной шкале температур.
– давление при измеряемой температуре. Таким образом, переходим к абсолютной шкале температур.
a) Предмет молекулярной физики. б) Основные положения МКТ. в) Статистический Подход описанию молекулярных явлений. г) Понятие о статистических закономерностях.
а) Термодинамика и молекулярная физика изучают макроскопические процессы в телах, связанные с колоссальным количеством молекул и атомов. Молекулярная физика исходит из представления об атомно-молекулярном строении вещества и рассматривает теплоту как беспорядочное движение атомов и молекул. Рассматривает свойства и строение отдельных атомов и молекул.
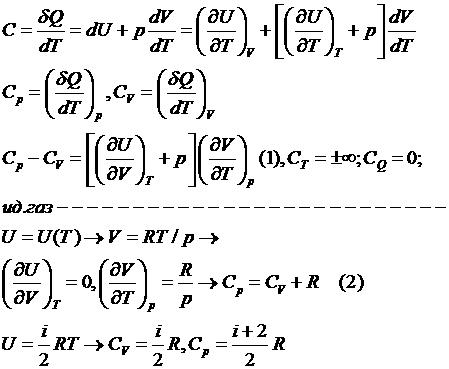 б) Газ разряжен, молекулы – упругие шарики (материальные точки), обладающие только кинетической энергией.
б) Газ разряжен, молекулы – упругие шарики (материальные точки), обладающие только кинетической энергией.
в) Для изучения системы многих частиц информация должна иметь обобщённый характер и относится не к отдельным частицам, а к совокупности большого числа частиц – статистический метод. Законы поведения совокупностей большого числа частиц, исследуемые статистическими методами, называются статистическими закономерностями.
г) Закономерности, обусловленные массовостью участвующих в их возникновении ингредиентов, называются статистическими, (бросание монеты).
а) Теплоёмкость системы. б) Теплоёмкость идеального газа в) Связь теплоёмкости газа с числом степеней свободы молекул. г) Уравнение Майера.
а) Теплоёмкость является характеристикой бесконечно малого процесса, совершаемого телом. ![]() – функция состояния.
– функция состояния.
б) Уравнение ![]() – уравнение Майера, выражает соотношение теплоёмкостей в идеальном газе.
– уравнение Майера, выражает соотношение теплоёмкостей в идеальном газе.
Термодинамический подход включает в себя следующие положения: термодинамика не вводит никаких специальных гипотез и конкретных представлений о строении вещества и физической природе теплоты. Ее выводы основаны на общих принципах, являющихся обобщением опытных фактов. Она рассматривает теплоту как внутреннее движение, но не пытается конкретизировать, что это за движение (ср. с билетом 1). Термодинамическое равновесие трудно поддается логическому определению. К нему приходят при рассмотрении конкретных реальных явлений последующего обобщения. Например: 2 тела при тепловом контакте в изолированной системе при разных температурах.
Квазистатические процессы – идеализированные процессы, состоящие из непрерывно следующих друг за другом состояний равновесия. Если в результате какого-либо процесса система переходит из состояния ![]() в другое состояние
в другое состояние ![]() и если возможно ее вернуть хотя бы одним способом в исходное состояние
и если возможно ее вернуть хотя бы одним способом в исходное состояние ![]() , притом так, чтобы во всех остальных телах не произошло никаких изменений, то процесс – обратимый, иначе – необратимый. Если способ возврата безразличен, то процесс обратимый в широком смысле слова, а если через ту же последовательность, то – в узком смысле слова. Квазистатические процессы обратимы в узком смысле слова.
, притом так, чтобы во всех остальных телах не произошло никаких изменений, то процесс – обратимый, иначе – необратимый. Если способ возврата безразличен, то процесс обратимый в широком смысле слова, а если через ту же последовательность, то – в узком смысле слова. Квазистатические процессы обратимы в узком смысле слова.
Поможем написать любую работу на аналогичную тему

