ПВК, окисляется с участием коэнзима А до ацетил-КоА. В данном процессе работают ферменты пируватдегидрогеназы: CH3–CO–COOH + KoA–SH + HAД+ = CH3–CO~KoA + НАД · Н2 + CO2
Ацетил-КоА является исходным субстратом цикла трикарбоновых кислот (ЦТК), или цикла Кребса.
В цикл Кребса включается одна молекула ацетил-КоА, которая в реакции с оксалоацетатом, катализируемой цитратсинтетазой, приводит к образованию лимонной кислоты и свободн. коэнзимаА. Лимонная кислота с помощью фермента аконитазы превращается в цис-акотиновую и изолимонную кислоты. Изолимонная кислота через щавелевоянтарную кислоту превращается в а-кетоглутаровую кислоту, которая подвергается дальнейшему декарбоксилированию.
В конечном итоге - двух молекул СО2, одной молекулы АТФ и 8 атомов водорода, из которых шесть атомов связаны в молекулах пиридиннуклеотидов и два атома – в молекулах флавопротеинов.
У некоторых бактерий цикл трикарбоновых кислот «разорван». Наиболее часто отсутствует этап превращения а-кетоглутаровой кислоты в янтарную. В таком виде ЦТК не может функционировать в системе энергодающих реакций клетки. Основная функция «разорванного» ЦТК – биосинтетическая.
Образовавшиеся на разных этапах окисления органических веществ НАДН2 и ФАДН2, поступают в дыхательную цепь, которая у бактерий находится в цитоплазматической мембране. Они вновь окисляются до НАД и ФАД, а отщепившийся от них водород передается не менее чем через пять переносчиков на заключительный участок цепи, где соединяется с молекук.кислородом, образуя воду.
Транспорт водорода сопровождается протеканием ряда окислительно-восстановительных реакции- образ.АТФ - окислительного фосфорилирования.
Флавопротеины – коферменты, в состав которых входит витамин В2, а в качестве простетических групп в них выступают флавинмононуклеотид (ФМН) или флавинадениндинуклеотид (ФАД). Флавопротеины осуществляют перенос атомов водорода, т. е. являются дегидрогеназами. Дегидрогеназа, содержащая в качестве простетической группы ФМН, яв- ляется НАДФН2-дегидрогеназой. Это стартовый переносчик в дыхательной цепи, осуществляющей перенос водорода с НАДФН2 на следующие компоненты дыхательной цепи. Дегидрогеназа, содержащая в качестве простетической группы ФАД, действует как сукцинатдегидрогеназа. Она катализирует окисление янтарной кислоты в фумаровую в ЦТК. Атомы водорода от ФАДН2 поступают сразу на хиноны, локализ. на последних этапах электронтрансп.ц.
Железосерные белки (FeS-белки) содержат железосероцентры, в которых атомы железа связаны, с одной стороны, с серой аминокислоты цистеина, а с другой – с неорганической сульфидной серой.
Железосероцентры входят в состав некоторых флавопротеинов или же служат в качестве единственных простетических групп белков. Железосероцентры в зависимости от строения могут осуществлять одновременный перенос одного или двух электронов, что связано с изменением валент. атомов железа.
Хиноны – жирорастворимые соединения. У грамотрицательных бактерий они представлены убихиноном (кофермент Q) или менахиноном
Хиноны липофильны, и поэтому локализуются в липидной фазе мембраны. Они переносят атомы водорода. Они служат «сборщиками» водорода, поставляемого различными коферментами и простетическими группами в дыхательной цепи, и передают его цитохромам.
Цитохромы принимают участие на заключительном этапе в цепи переноса электронов. К ним электроны поступают от хинонов. В качестве простетической группы цитохромы содержат гем. Цитохромы окра-
шены; они отличаются друг от друга спектрами поглощения и окислительно-восстановительными потенциалами. Широко распространен цитохром с. Конечные (терминальные) цитохромы дыхательной цепи – это цитохромы а + а3 или цитохромоксидаза. Они передают электроны на молекулярный
кислород, т. е. катализируют восстановление молекулярного кислорода до воды. В реакционном центре цитохромоксидазы, помимо двух гемов, содержатся два атома меди.
Флавопротеины и хиноны осуществляют перенос атомов водорода, а FeS-белки и цитохромы – электронов.
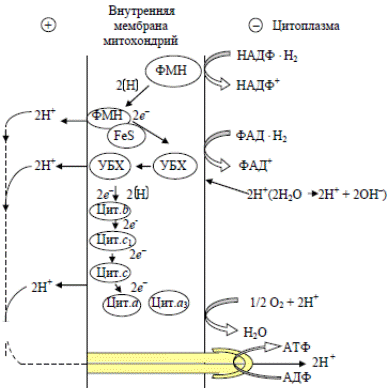 у дрожжей: • комплекс 1 – НАД Н2-дегидрогеназа; в него входят ФМН и железосерные белки; НАД Н2-дегидрогеназа переносит водород от НАДН2 к коферменту Q; • комплекс 2 – сукцинатдегидрогеназа, содержащая ФАД. Она отдает водород в дыхательную цепь на уровне кофермента Q; • комплекс 3 – цитохром b и цитохром с1, принимающие электроны от кофермента Q и передающие их на цитохром с; • комплекс 4 –цитохромоксидаза, осуществляющая перенос электронов на молекулярный кислород.
у дрожжей: • комплекс 1 – НАД Н2-дегидрогеназа; в него входят ФМН и железосерные белки; НАД Н2-дегидрогеназа переносит водород от НАДН2 к коферменту Q; • комплекс 2 – сукцинатдегидрогеназа, содержащая ФАД. Она отдает водород в дыхательную цепь на уровне кофермента Q; • комплекс 3 – цитохром b и цитохром с1, принимающие электроны от кофермента Q и передающие их на цитохром с; • комплекс 4 –цитохромоксидаза, осуществляющая перенос электронов на молекулярный кислород.
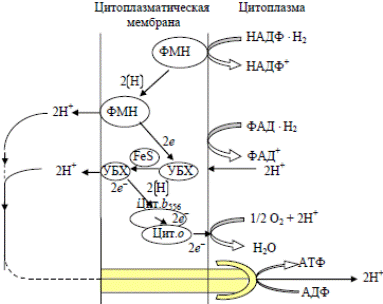
Дых. цепь бактерий E. coli: - в нее не входит цитохром с; - дых. цепь у E. coli разветвлена.
В клетках, растущих в условиях достаточной аэрации, восстановительные эквиваленты передаются к кислороду преимущественно через кофермент Q, цитохром b556 и цитохром о. При ограниченном снабжении кислородом клетки используют в качестве переносчиков электронов менахинон или убихинон и цитохромы b558 и d. В последнем случае обр-ся меньшее АТФ.
У дрожжей существуют 3 пункта фосфорилирования, которые соответствуют участкам
выхода протонов во внешнюю среду. Первый участок локализован в на-чале дыхательной цепи и связан с функционированием НАДФН2-дегидрогеназы. Второй определяется способностью убихинона переносить водород. Последний локализован в конце цепи и связан с активностью цитохромоксидазы.
Так как внутренняя мембрана митохондрий и цитоплазматическая мембрана бактерий непроницаемы для ионов, в том числе и для Н+, и ОН–, то создается трансмембранный электрохимический, или протонный градиент между наружной и внутренней их сторонами. Протоны могут обратно поступать
через мембрану только в определенных местах. В них располагаются АТФ-синтазы.
 Установлено, что синтез молекулы АТФ связан с переносом двух протонов через комплекс АТФ-синтазы. При окислении НАДН2 молек. кислородом выделяется 6 протонов,макс.выход АТФ =3.
Установлено, что синтез молекулы АТФ связан с переносом двух протонов через комплекс АТФ-синтазы. При окислении НАДН2 молек. кислородом выделяется 6 протонов,макс.выход АТФ =3.
• в процессе гликолиза образуются 2 АТФ, 2 НАДН2 и 2пирувата; • при окислительном декарбоксилировании 2 пирувата образуются 2 ацетил-КоА и 2 НАДН2; • окисление 2 ацетил-КоА в цикле Кребса приводит к образованию 6 НАДН2, 2 ФАДН2 и 2 АТФ. НАДН2 - 3 АТФ, ФАДН2 – 2 АТФ.Суммарный энергетический выход С6Н12О6 + 6О2 + 38АДФ + 38Н3РО4 6СО2 + 38АТФ + 44Н2О
E. coli. Имеются только два пункта, в которых происходит «выброс» протонов.Следовательно, при окислении одной молекулы НАДН2 образуются только 2 АТФ, а при окисл. молекулы ФАДН2 – 1 АТФ. E. coli 26 молекул АТФ: • 2 АТФ синтезируются в гликолизе; • 2 АТФ синтезируются в двух оборотах цикла Кребса; • 10 молекул НАДН2 приводят к синтезу 20 молекул АТФ; • 2 ФАДН2=2 АТФ.
Corynebacterium diphtheriae имеется только один пункт «выброса» протонов. У Mycobacterium phlei – 3.
Поможем написать любую работу на аналогичную тему

