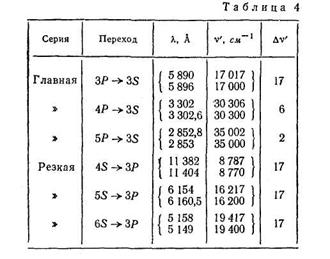
Исследование спектров щелочных металлов при помощи приборов с большой разрешающей силой показало, что каждая линия этих спектров является двойной (дублет). Так, например, характерная для натрия желтая линия ЗР ![]() 3S состоит из двух линий с длинами волн 5890 А и 5896 А. То же относится и к другим линиям главной серии, а также к линиям других серий. В табл. 4 приведены некоторые дублеты натрия. В четвертом столбце указаны волновые числа линий
3S состоит из двух линий с длинами волн 5890 А и 5896 А. То же относится и к другим линиям главной серии, а также к линиям других серий. В табл. 4 приведены некоторые дублеты натрия. В четвертом столбце указаны волновые числа линий ![]() '. В последнем столбце дано расщепление компонент дублетов (разность волновых чисел).
'. В последнем столбце дано расщепление компонент дублетов (разность волновых чисел).
Расщепление спектральных линий, очевидно, обусловлено расщеплением энергетических уровней. Поскольку расщепление линий главной серии nP![]() 3S различно, а для линий резкой серии nS
3S различно, а для линий резкой серии nS![]() 3P одно и то же
3P одно и то же
(см. табл. 4), приходится предположить, что уровни S являются одиночными (синглетами), а уровни Р — двойными (дублетными) (см. рис. 204). Дальнейший анализ спектра натрия показал, что уровни D и F также являются двойными.
Структура спектра, отражающая расщепление линий на компоненты, называется тонкой структурой. Сложные линии, состоящие из нескольких компонент, получили название мультиплетов. Тонкая структура обнаруживается, кроме щелочных металлов, также и у других элементов, причем число компонент в муль-типлете может быть равно двум (дублеты), трем (триплеты), четырем (квартеты), пяти (квинтеты) и т. д. В частном случае спектральные линии даже с учетом тонкой структуры могут быть одиночными (синглеты).
Для объяснения мультиплетной структуры спектров и аномального эффекта Зеемана Гаудсмит и Юленбек выдвинули в 1925 г. гипотезу о том, что электрон обладает собственным моментом импульса Ms, не связанным с движением электрона в пространстве. Этот собственный момент был назван спином.
Первоначально предполагалось, что спин обусловлен вращением электрона вокруг своей оси. Согласно этим представлениям электрон уподоблялся волчку или веретену. Кстати, отсюда происходит и сам термин «спин»: по-английски spin означает «верчение». Однако очень скоро пришлось отказаться от подобных модельных представлений, в частности по следующей причине. Вращающийся заряженный шарик должен обладать магнитным моментом, причем отношение магнитного момента к механическому должно иметь значение : ![]() (1)
(1)
Действительно, было установлено, что электрон, наряду с собственным механическим моментом, обладает также и собственным магнитным моментом ![]() . Однако ряд опытных фактов, в частности аномальный эффект Зеемана, свидетельствует о том, что отношение собственных магнитного и механического моментов в два раза больше, чем для орбитальных моментов:
. Однако ряд опытных фактов, в частности аномальный эффект Зеемана, свидетельствует о том, что отношение собственных магнитного и механического моментов в два раза больше, чем для орбитальных моментов: ![]() (2)
(2)
Таким образом, представление об электроне как о вращающемся шарике оказалось несостоятельным. Спин следует считать внутренним свойством, присущим электрону подобно тому, как ему присущи заряд и масса.
Предположение о спине электрона было подтверждено большим количеством опытных фактов и должно, считаться совершенно доказанным. Оказалось также, что наличие спина и все его свойства автоматически вытекают из установленного Дираком уравнения квантовой механики, удовлетворяющего требованиям теории относительности. Таким образом, выяснилось, что спин электрона является свойством одновременно квантовым и релятивистским. В настоящее время также установлено, что спином обладают и другие элементарные частицы: протоны, нейтроны, фотоны и др.
Величина собственного момента импульса электрона определяется по общим законам квантовой механики так называемым спиновым квантовым числом s, равным 1/2: ![]() . (3)
. (3)
Составляющая механического момента по заданному направлению может принимать квантованные значения, отличающиеся друг от друга на h:
![]() где
где ![]() (4)
(4)
Чтобы найти величину собственного магнитного момента электрона, умножим Ms на отношение (2) ![]() к Ms:
к Ms:
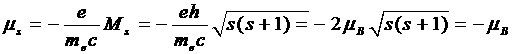 . (5)
. (5)
Знак минус указывает на то, что механический Ms и магнитный ц,5 моменты электрона направлены в противоположные стороны.
Проекция собственного магнитного момента электрона на заданное направление может иметь следующие значения:
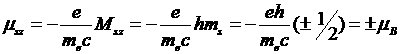
(минус получается, если ms = + ![]() , плюс — если ms = = -
, плюс — если ms = = -![]() ).
).
Таким образом, проекция собственного момента импульса электрона может принимать значения +![]() и -
и -![]() , а собственного магнитного момента — значения +
, а собственного магнитного момента — значения + ![]() и .
и .![]() В ряд формул, в частности в выражение для энергии, входят не сами моменты, а их проекции. Поэтому принято говорить, что собственный механический момент (спин) электрона равен половине (подразумевается в единицах h), а собственный магнитный момент равен одному магнетону Бора.
В ряд формул, в частности в выражение для энергии, входят не сами моменты, а их проекции. Поэтому принято говорить, что собственный механический момент (спин) электрона равен половине (подразумевается в единицах h), а собственный магнитный момент равен одному магнетону Бора.
Рассмотрим теперь на примере атома натрия, как существование спина электрона может объяснить мультиплетную структуру спектра. Поскольку момент атомного остатка равен нулю, момент атома натрия равен моменту оптического электрона. Момент же электрона будет слагаться из двух моментов: орбитального Mi, обусловленного движением электрона в атоме, и спинового Ms, не связанного с движением электрона в пространстве. Результирующая этих двух моментов дает полный момент импульса оптического электрона. Сложение орбитального и спинового моментов в полный момент осуществляется по тем же квантовым законам, по которым складываются орбитальные моменты разных электронов. Величина полного момента Mj определяется квантовым числом j:
![]() причем / может иметь значения:
причем / может иметь значения: ![]()
где l и s соответственно азимутальное и спиновое квантовые числа. При l=0 квантовое число j имеет только одно значение: j = s = ![]() . При l, отличном от нуля, возможны два значения: j = l +
. При l, отличном от нуля, возможны два значения: j = l +![]() и j = l-
и j = l-![]() , которые соответствуют двум возможным взаимным ориентациям моментов Ml и Ms — «параллельной» и «антипараллельной».
, которые соответствуют двум возможным взаимным ориентациям моментов Ml и Ms — «параллельной» и «антипараллельной».
Теперь учтем, что с механическими моментами связаны магнитные моменты, которые взаимодействуют друг с другом подобно тому, как взаимодействуют два тока или две магнитные стрелки. Энергия этого взаимодействия (называемого спин-орбитальным взаимодействием) зависит от взаимной ориентации орбитального и собственного моментов. Следовательно, состояния с различными j должны обладать различной энергией.
Таким образом, каждый терм ряда Р(l=1) расщепляется на два, соответствующих j = ![]() и j = 3/2; каждый терм ряда D (l = 2) расщепляется на термы с j = 3/2 и j =
и j = 3/2; каждый терм ряда D (l = 2) расщепляется на термы с j = 3/2 и j = ![]() , и т. д. Каждому терму ряда S(l= 0) соответствует только одно значение j=
, и т. д. Каждому терму ряда S(l= 0) соответствует только одно значение j= ![]() ; поэтому термы ряда S не расщепляются.
; поэтому термы ряда S не расщепляются.
Итак, каждый ряд термов, кроме S, распадается на два ряда—структура термов оказывается дублетной (двойной). Термы принято обозначать символами:
|
|

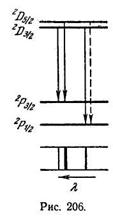
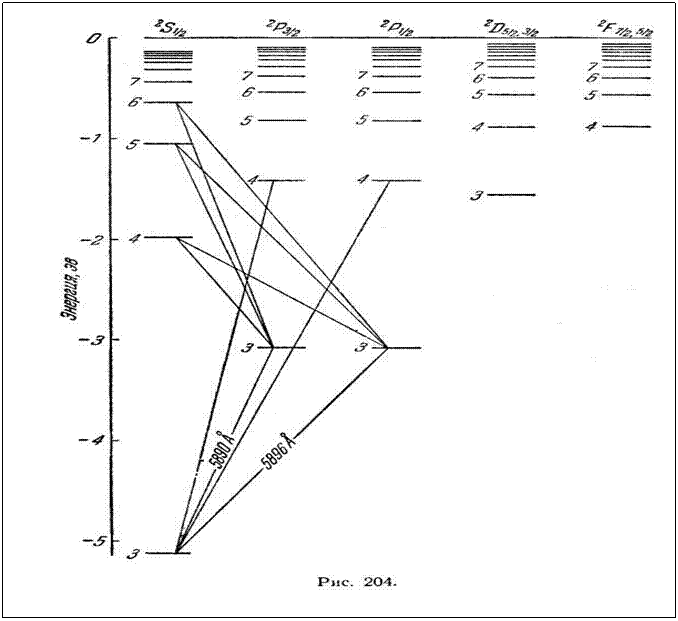
С учетом тонкой структуры схема термов выглядит более сложно, о чем дают представление схемы уровней натрия (рис. 1) и цезия (рис. 2). Поскольку мультиплетное расщепление термов D и F для натрия очень мало, подуровни D и F, отличающиеся значениями /, изображены на схеме слитно. Мультиплетное расщепление у цезия значительно больше, чем у натрия. На схеме цезия видно, что тонкая структура диффузной серии состоит не из двух линий, а из трех:
![]()
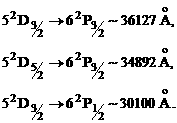
|
|
Возникновение этих линий пояснено дополнительно на рис. 206, Изображенный пунктиром переход ![]() запрещен правилом отбора:
запрещен правилом отбора:
![]() = 0, ±1. (7)
= 0, ±1. (7)
В нижней части схемы на рис. 3 показано, как выглядит сам мультиплет. Толщина линий на, схеме примерно соответствует" интенсивности спектральных линий. Совокупность получающихся линий выглядит как дублет, у которого одна из компонент в свою очередь оказывается двойной. Такая группа линий называется не триплетом, а сложным дублетом, так как она возникает в результате комбинации дублетных термов.
|
Поможем написать любую работу на аналогичную тему