Всякая жидкость ( и смесь жидкостей) кипит когда давление её паров становится равным атмосферному давлению. Испарение происходит при любой температуре.
Чем больше давление паров жидкости, тем она быстрее закипает ( при более низкой температуре).
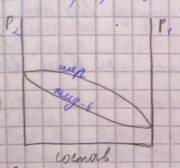 Кривая «пар», выражает зависимость давления пара от состава пара. Кривая «жидкость» выражает зависимость давления пара от состава жидкости. Состав пара отличается от состава жидкости, кроме азиатропного раствора.
Кривая «пар», выражает зависимость давления пара от состава пара. Кривая «жидкость» выражает зависимость давления пара от состава жидкости. Состав пара отличается от состава жидкости, кроме азиатропного раствора.
Коновалов установил закон: Паровая фаза всегда обогащена более летучими компонентами.
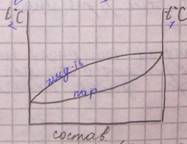 Вторая жидкость имеет более высокое давление пара, поэтому кипит при более низкой температуре.
Вторая жидкость имеет более высокое давление пара, поэтому кипит при более низкой температуре.
Кривая «жидкость» выражает зависимость температуры кипения смеси от состава жидкости. А кривая «пар» выражает зависимость температуры кипения от состава пара.
Азеотропные растворы – в переводе на русский язык, означают постоянно кипящие.
Азеотропные растворы это смеси двух жидкостей, но кипят они при постоянной температуре, то есть как чистая жидкость. ( или это раствор двух жидкостей, определённого состава)
Азеотропный раствор, обладающий максимальным давлением пара, кипит при более низкой температуре, чем растворы иного состава ( из тех же жидкостей).
Азеотропный раствор, обладающий минимальным давлением пара, кипит при более высокой температуре, чем растворы иного состава. Эти выводы сделал Коновалов.
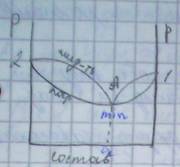
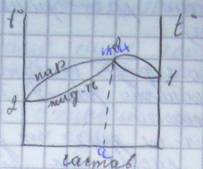
рис1 (а) рис 1 (б)
При сильном отрицательном отклонении от линии зависимости, на кривой давление пара появляется точка минимум, а на кривой температура кипения – точка максимума. Точка А – азеотропный раствор.
Кривая «пар» и кривая «жидкость» в точке А смыкаются, потому что для азеотропного раствора, состав жидкости совпадает с составом пара.
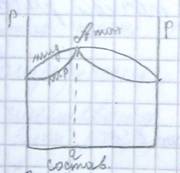
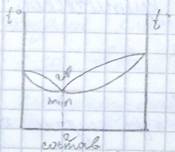
рис 2 (а) рис 2 (б)
Азеотропный раствор с максимальным давлением пара имеет минимальную температуру кипения.
При сильном положительном отклонении от линейной зависимости, на кривой давления пара появляется точка максимума, ей соответствует точка минимума температуры кипения.
Каким бы не был тип отклонения азеотропных смесей, им присуще одно общее свойство: в точках экстремума, на диаграммах давления и кипения составы жидкой и газовой фаз смеси одинаковы. Это и есть второй закон Коновалова.
Поможем написать любую работу на аналогичную тему
Реферат
Тип диаграмм «состав – давление пара», «состав – температура кипения». Азеотропы. Первый и второй закон Коновалова – Гиббса.
От 250 руб
Контрольная работа
Тип диаграмм «состав – давление пара», «состав – температура кипения». Азеотропы. Первый и второй закон Коновалова – Гиббса.
От 250 руб
Курсовая работа
Тип диаграмм «состав – давление пара», «состав – температура кипения». Азеотропы. Первый и второй закон Коновалова – Гиббса.
От 700 руб

