Аминокислоты - строительные блоки белков. Общее строение, физико-химические свойства аминокислот
COOH
I
H2Na -C-H
I
R
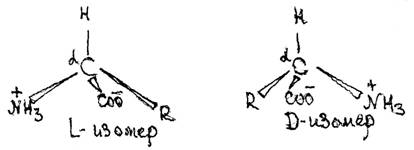
L-Форма
Строительными блоками белков служат 20 различных, но весьма сходных по строению, аминокислот, все они содержат аминную (NН2), карбоксильную (-СООН), радикальную (R-) группы и атом водорода связанные с ассиметричным a-углеродным атомом. Аминокислоты отличаются друг от друга строением R-группы. Все аминокислоты, за исключением глицина, оптически активны и могут существовать в виде L- и D- формы. В составе белков всех организмов обнаруживаются только a-аминокислоты L - ряда. D - формы аминокислот встречаются редко, в составе клеточных стенок некоторых микроорганизмов, пептидных антибиотиков, организмами животных и растений не усваиваются.
В водных растворах при рН близких к физиологическим (от б до 8) a-аминокислоты превращаются в биполярные ионы, т.к. a-СООН (кислая) группа диссоциирует, отдавая протон (Н+), заряжается отрицательно;
a-NH2 (щелочная) группа принимает протон (протонируется) и заряжается положительно:
COO- Биполярность молекул обуславливает хорошую
I растворимость большинства аминокислот в воде. В
H3![]() a-C -H кислых растворах (при рН 6-1) аминокислоты
a-C -H кислых растворах (при рН 6-1) аминокислоты
I присутствуют в виде положительных ионов, а в
R щелочных (рH 8-I2) - в виде отрицательных ионов, т.е. аминокислоты являются амфотерными веществами с буферными свойствами.
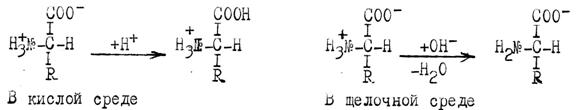 |
Важнейшим свойством a-аминокислот является их способность конденсироваться, соединяться между собой пептидной связью (-СО-NН-), которая образуется при взаимодействии a-СОО- группы первой аминокислоты с a![]() H3 группой второй аминокислоты с отщеплением Н2О:
H3 группой второй аминокислоты с отщеплением Н2О:
R1 R1
![]()
![]() ï ï
ï ï
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() + CH + COO- + CH NH COO-
+ CH + COO- + CH NH COO-
![]()
![]() H3N COO- + H3N-CH H3N CO CH
H3N COO- + H3N-CH H3N CO CH
ï -H2O ï
R2 R2
Поможем написать любую работу на аналогичную тему

