Большинство глобулярных белков - это гидрофильные вещества, хорошо растворяющиеся в водных растворах, т.к. основная часть поверхности их молекул образована полярными группами, способными гидратироваться.
Под гидратацией понимают ориентированное связывание диполей воды полярными (+) и (-) заряженными R-группами за счёт электростатических (ион-дипольных) взаимодействий с образованием прочных гидратных оболочек.
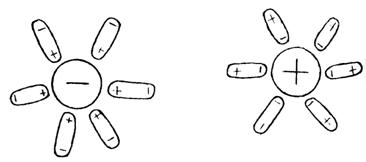 |
Ион- дипольные (электростатические) взаимодействия между
заряженной молекулой белка и диполями воды.
Степень гидратации различных молекул не одинакова, зависит от их размеров и величины заряда. Чем выше удельная плотность заряда (больше заряд и меньше размеры) тем сильнее гидратация.
Гидратные оболочки препятствуют агрегации белковых молекул. Таким образом, заряды и гидратные оболочки молекул белка, являются важными факторами устойчивости белковых растворов.
Растворимость белков в воде (диэлектрическая постоянная молекул воды при комнатной температуре = 80, у ацетона, этанола-20-30) возрастает при небольших концентрациях нейтральных солей (NaCl, MgSO4,(NH4)2SO4 и др.), т.к. нейтральные соли в малых концентрациях увеличивают диэлектрическую постоянную воды. В результате вода усиливает диссоциацию R-COOH и протонирование R-NH2 групп молекул белка; диполи воды образуют вокруг заряженных R-+NH3 и R-COO- групп гидратные оболочки, которые уменьшают взаимодействие между молекулами белков.
Высокие концентрации нейтральных солей, напротив, осаждают (высаливают) белки из водных растворов, т. к, ионы солей оттягивают "на себя" с заряженных групп белка диполи воды и частично или полностью лишают белок гидратной оболочки, увеличивают ионные взаимодействия между молекулами с образованием крупных агрегатов белка, выпадающих в осадок.
Добавление к белковому раствору этанола, ацетона и др. органических растворителей уменьшает растворимость белков, а при больших концентрациях наблюдается выпадение белков в осадок. Это объясняется снижением диэлектрической постоянной воды и уменьшением степени гидратации белков, что приводит к увеличению притяжения между противоположно заряженными группами молекул белков, их агрегации (слипанию) и вьпадению в осадок.
Поможем написать любую работу на аналогичную тему

