Первое начало термодинамики для бесконечно малых величин может быть записано в виде:
![]() .
.
Внутренняя энергия: ![]() т.е. это среднее значение микроскопической внутренней энергии
т.е. это среднее значение микроскопической внутренней энергии
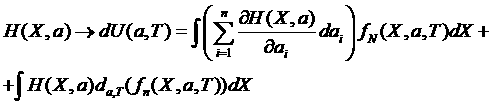 (*),
(*),
где ![]() – дифференциал по а и Т.
– дифференциал по а и Т.
Введем микроскопические (зависит от Х) силы, соответствующие обобщенным координатам ![]() :
:
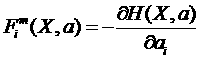 .
.
Отметим, что размерность этих сил может быть различной в зависимости от параметров ![]() .
.
Термодинамические силы ![]() определяются как средние от микроскопических сил:
определяются как средние от микроскопических сил: ![]() .
.
Работа в термодинамике может быть определена как:
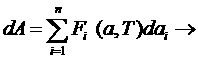
первый член (*) равен работе термодинамических сил
![]()
![]() (**).
(**).
Вполне понятно, что работа связана с изменением внешних параметров, поскольку они не дают вклада в кинетическую энергию, то должны дать вклад в потенциальную.
То есть ![]() определяется изменением функции распределения вследствие изменения термодинамических переменных а, Т.
определяется изменением функции распределения вследствие изменения термодинамических переменных а, Т.
Из условия нормировки:
![]()
![]() . (***)
. (***)
В выражении (**) разделим и умножим на ![]() и вычтем выражение
и вычтем выражение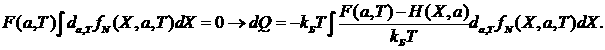
Используем каноническое распределение Гиббса:
![]() с учетом
с учетом ![]() – вынесем за интеграл
– вынесем за интеграл ![]() →(***).
→(***).
![]() .
.
Из определения энтропии в термодинамике: ![]() .
.
Если приравнять величину ![]() в каноническом распределении Гиббса к термодинамической температуре, то, сравнивая
в каноническом распределении Гиббса к термодинамической температуре, то, сравнивая ![]() , получим:
, получим:
![]() ,
,
где ![]() –константа, которая может быть определена только в квантовой статистической теории. Или:
–константа, которая может быть определена только в квантовой статистической теории. Или: ![]() .
.
Из термодинамики свободная энергия определяется как:
![]() .
.
Таким образом, действительно функция ![]() в каноническом распределении Гиббса совпадает со свободной энергией, определенной в термодинамике. Зная сводную энергию, можно вычислить основные термодинамические параметры:
в каноническом распределении Гиббса совпадает со свободной энергией, определенной в термодинамике. Зная сводную энергию, можно вычислить основные термодинамические параметры:
![]() .
.
Отсюда:
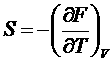 ,
, 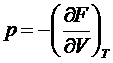 .
.
С другой стороны можно определить теплоемкость:
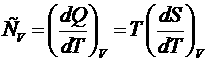 .
.
Таким образом, основной алгоритм, на котором основана равновесная СФ, выглядит так:
![]() .
.
Поможем написать любую работу на аналогичную тему
Реферат
Первое начало термодинамики с точки зрения статистической физики. Статистическое определение энтропии
От 250 руб
Контрольная работа
Первое начало термодинамики с точки зрения статистической физики. Статистическое определение энтропии
От 250 руб
Курсовая работа
Первое начало термодинамики с точки зрения статистической физики. Статистическое определение энтропии
От 700 руб

