Определение энтропии получено для![]() – канонического распределения Гиббса. Для произвольной функции распределения
– канонического распределения Гиббса. Для произвольной функции распределения ![]() введем энтропию (опуская
введем энтропию (опуская ![]() ):
):
![]()
(квадратные скобки означают, чтовеличина ![]() определена для совокупности случайной величин Х),
определена для совокупности случайной величин Х),
![]() .
.
Это для непрерывной переменной. Во многих случаях (в частности, в квантовой теории) используются функции распределения случайных величин, принимающих дискретный ряд значений n
(например, набор квантовых чисел). Обозначим соответствующую функцию ![]() . Тогда:
. Тогда: ![]() .
.
Тогда энтропия для дискретного распределения может быть представлена в виде
![]() .
.
Свойства ![]() и
и ![]()
1. Если ![]() при
при ![]() , и нулю для всех остальных значений, то
, и нулю для всех остальных значений, то ![]() . Это соответствует нулевой неопределенности задания состояния системы.
. Это соответствует нулевой неопределенности задания состояния системы.
2. Если число возможных значений дискретной переменной ![]() равно
равно ![]() и все возможные значения равновероятны:
и все возможные значения равновероятны: ![]() ,
, ![]() ,
, 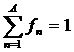 (–доказать).
(–доказать).
То можно показать, что ![]() в этом случае максимальна и равна:
в этом случае максимальна и равна:
![]() .
.
В таком виде формула для энтропии была получена еще Больцманом.
Это соответствует полному хаосу (максимальной неопределенности) задания состояния системы.
Для энтропии непрерывных величин ![]() результаты аналогичны.
результаты аналогичны.
Для сравнения найдем энтропию, соответствующую квантовому микроканоническому распределению Гиббса:
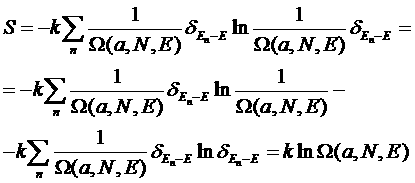 .
.
Второе слагаемое равно нулю, поскольку содержит 0ln0 или 1ln1. Таким образом, мы снова получаем формулу для энтропии в виде:
![]() .
.
Следовательно, энтропия может служить мерой неопределенности при статистическом описании процессов в макротелах.Такое определение энтропии можно использовать и для исследования неравновесных процессов, когда ![]()
![]() .
.
Третье начало термодинамики с точки зрения статистической физики
На основе анализа экспериментов Вальтер Нернст (1906 г.) пришел к выводу, что разность энтропий ![]() соответствующих любым двум модификациям вещества стремиться к нулю при приближении к нулю абсолютной температуры:
соответствующих любым двум модификациям вещества стремиться к нулю при приближении к нулю абсолютной температуры: ![]() .
.
Позднее Планк сформулировал Результат Нернста в еще более определенной форме: ![]() при
при ![]() – теорема Нернста (третье начало).
– теорема Нернста (третье начало).
Из нее следует ряд термодинамических следствий. Обратимся к квантовому каноническому распределению Гиббса. Из него следует выражение для энтропии: ![]()
![]() .
.
Из квантового канонического распределения Гиббса следует, что наиболее вероятным является квантовое состояние системы с наименьшим возможным значением энергии – основное состояние.
В равновесном состоянии функция распределения ![]() максимальна для основного состояния. Если через
максимальна для основного состояния. Если через ![]() обозначить разность энергий основного и возбужденного состояний, то при температуре
обозначить разность энергий основного и возбужденного состояний, то при температуре ![]() вероятность функции
вероятность функции ![]() для основного состояния будет близка к единице, а при Т=0:
для основного состояния будет близка к единице, а при Т=0: 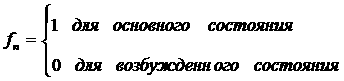
Эта функция удовлетворяет условию нормировки.
Действительно, записывая условие нормировки в виде:
![]() ,
,
получим
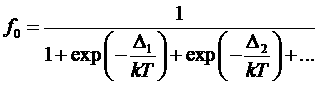 .
.
При таком распределении все члены выражения для ![]() равны нулю
равны нулю ![]() при
при ![]() .
.
Таким образом, третье начало с точки зрения статистической физики можно сформулировать так:
при ![]() система находится только в основном состоянии, поэтому неопределенность задания состояния равна нулю. Этому соответствует равенство нулю энтропии, которая является мерой неопределенности состояния при статистическом описании.
система находится только в основном состоянии, поэтому неопределенность задания состояния равна нулю. Этому соответствует равенство нулю энтропии, которая является мерой неопределенности состояния при статистическом описании.
Поможем написать любую работу на аналогичную тему
Реферат
Энтропия – мера неопределенности при статистическом описании. Статистическое обоснование третьего начала термодинамики
От 250 руб
Контрольная работа
Энтропия – мера неопределенности при статистическом описании. Статистическое обоснование третьего начала термодинамики
От 250 руб
Курсовая работа
Энтропия – мера неопределенности при статистическом описании. Статистическое обоснование третьего начала термодинамики
От 700 руб

